伤口愈合是很常见的。然而,延迟愈合和异常疤痕导致病理性伤口愈合。因此,无疤痕伤口愈合仍然是一个重大的临床挑战。在这项研究中,我们构建了透明质酸(HA)修饰和维托酚芬(VP)负载的聚乳酸(PLA)纳米凝胶(HA/VP-PLA),通过加速伤口再上皮化和控制疤痕形成来促进无疤痕伤口愈合。由于HA与VP-PLA纳米颗粒的独特结构,HA/VP-PLA可以局部涂抹在伤口上,实现成纤维细胞的靶向递送。然后,HA/VP- pla释放HA和乳酸(LA)刺激成纤维细胞增殖和迁移,释放VP抑制Yes-associated protein (YAP)表达和核定位,抑制纤维化。体外(皮肤成纤维细胞)和体内(大鼠和家兔模型)实验强烈表明,HA/VP-PLA通过加速创面再上皮化和控制瘢痕形成来促进无疤痕创面愈合。因此,我们的工作为无疤痕伤口愈合提供了一种可行的策略,并且复杂的HA/VP-PLA具有很大的临床应用潜力。
伤口愈合是人类常见的现象,多年来一直是一个活跃的研究领域[1,2]。它是一个极其复杂和协调的过程,包括四个连续的、重叠的生物阶段(止血、炎症、增殖和重塑),在这些阶段中受损组织得到恢复[3]。在创面愈合过程中,外部和内部因素的干扰可能导致不满意的结果,从而导致愈合延迟和异常瘢痕形成[3]。因此,迫切需要开发一种针对延迟愈合和异常疤痕的无疤痕伤口愈合方法。
伤口愈合的分子和细胞机制被广泛研究[4,5]。然而,实现完美的无疤痕伤口愈合仍然很困难。在成年人中,疤痕形成是伤口愈合的结果,其特征是皮肤增生,细胞外基质(ECM)致密,胶原蛋白紊乱[6]。最近,有报道称疤痕形成的机制是yes相关蛋白(YAP)的持续激活,YAP上调纤维化并导致过度的ECM沉积[7,8]。因此,抑制YAP可能是治疗各种纤维化疾病时抑制纤维化的一种治疗策略[9,10]。vertex porfin (VP)是美国食品和药物管理局(FDA)批准的卟啉化合物,已证实可抑制YAP表达,抑制纤维化并产生无疤痕皮肤再生[11,12]。因此,基于vpp的YAP抑制是控制瘢痕形成的候选机制,然而,抑制纤维化可阻止伤口再上皮化[13]。幸运的是,纳米技术的出现整合了加速伤口再上皮化和控制疤痕形成的能力。
最近,纳米技术为伤口愈合提供了新的机会,使用不同的策略来实现抗菌特性、药物传递和伤口微环境调节[14,15]。目前,聚(D, l -乳酸)(PLA)纳米颗粒(PLA NPs)已被批准用于生物医学应用,并作为伤口愈合的成功模式[16,17,18]。此外,乳酸(LA), PLA降解的产物,被认为通过刺激成纤维细胞增殖来加速伤口的再上皮化[19,20]。因此,PLA NPs与VP联合使用可通过加速创面再上皮化和控制瘢痕形成来促进无疤痕创面愈合。然而,将VP-PLA NPs (VP-PLA NPs)应用于伤口是具有挑战性的。
基于纳米凝胶的局部治疗是伤口愈合的经典方法[21,22]。纳米凝胶具有特定的亲水性3D大分子网络结构,具有优异的保水性能和胶体稳定性[23]。目前,透明质酸(HA)在纳米凝胶制剂中表现出优异的性能,通过刺激成纤维细胞的增殖和迁移来促进伤口愈合[24,25]。透明质酸是ECM中由n -乙酰氨基葡萄糖和d -葡萄糖醛酸组成的天然多糖,具有生物活性、生物相容性和可生物降解性。特别是,HA修饰的纳米颗粒已经被研究用于靶向递送到成纤维细胞,因为它们表达HA受体(如CD44)[26]。有趣的是,HA由于含有疏水和亲水斑块结构域而表现出两亲性[27]。CH基团的疏水斑块结构域有助于HA与PLA相互作用,并被纳入PLA NPs中。HS具有亲水性贴片结构域,可以提高PLA NPs的稳定性。此外,PLA NPs中的HA由于其水解降解特性而促进VP从PLA NPs中释放[28,29]。因此,HA修饰的VP-PLA NP纳米凝胶(HA/VP-PLA)可能通过加速伤口再上皮化和控制疤痕形成提供一种理想的无疤痕伤口愈合方法。
因此,制备了复杂的HA/VP-PLA,构成HA掺入和HA包被的VP-PLA NPs,用于无疤痕伤口愈合。HA/VP-PLA可靶向递送至成纤维细胞,释放HA和LA加速创面再上皮化,实现基于vp的YAP抑制,抑制纤维化,控制瘢痕形成(方案1)。HA/VP-PLA在抑制YAP、刺激成纤维细胞增殖和迁移方面表现出优异的性能。组织病理学分析表明,HA/VP-PLA在大鼠和家兔模型中均能加速创面再上皮化,控制瘢痕形成。因此,本研究提出了一种无疤痕伤口愈合的策略。
方案1
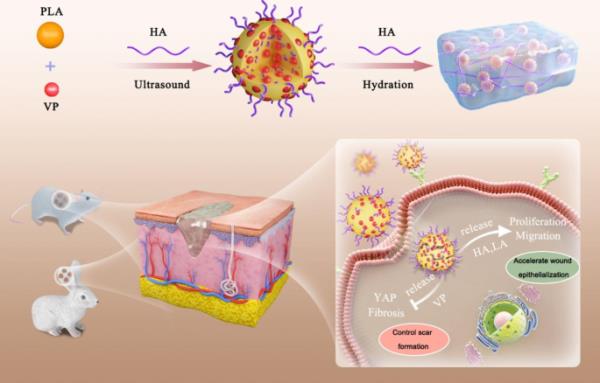
HA/VP-PLA通过加速创面再上皮化和控制瘢痕形成促进无疤痕创面愈合的示意图
采用纳米沉淀法制备了HA/VP-PLA。简单地说,将VP(16μg, Sigma-Aldrich)和PLA (40 mg,分子量47 kDa,带羧基,Sigma-Aldrich)在丙酮(1 mL)中逐渐加入10 mL HA (0.5 mg/mL, 1.0 MDa, Aladdin)乙醇水溶液(20%乙醇,v/v)中搅拌2 h,然后在30°C旋转蒸馏塔上蒸发有机溶剂,水溶液在超声波水浴中超声40 min, 300 W。HA/VP-PLA与HA (80 mg)水化过夜后得到。用类似的方法制备无VP纳米凝胶(PLA-HAs)和HA纳米凝胶中的VP (VP- has)。
采用透射电镜(TEM, JEM-2010,日本)、低温透射电镜(Cryo-TEM, Talos F200C G2,美国)、磷酸钨酸钠溶液(1.5% w/v, 20 s)阴性染色。扫描电子显微镜(SEM, JSM-6360LA,日本)。紫外-可见(UV-Vis)光谱使用Varian Cary 50紫外-可见分光光度计(Perkin Elmer,美国)获得。体外释放VP的方法是将500μL HA/VP- pla在5ml PBS中与10%胎牛血清(FBS,模拟生理条件)在37℃下孵育。样品的等分液(50μL)用于释放VP的荧光测定。捕获效率(EE)和VP释放量计算如下:
EE=VP分析权重/ VP理论权重x 100%。
VP释放=总VP释放/总VP增加x 100%。
因此,EE可以被认为等于VP释放。此外,根据前人的研究[30],将样品用高效液相色谱(HPLC)测定生成pla的LA。
用胶原酶消化法从包皮组织中分离出人皮肤成纤维细胞。收集过滤后的成纤维细胞,在含有胎牛血清(FBS, 10%)的Dulbecco改良鹰培养基中培养,每3天更换一次培养基。所有细胞在37°C、5% CO2、湿润气氛下培养。3-6代后将细胞用于后续实验。
动物实验经上海市第九人民医院动物实验伦理委员会批准(IACUC编号:SH9H-2021-A428-SB)。为了验证创面再上皮化,用2.5%异氟醚麻醉18只雄性Sprague Dawley大鼠(180-250 g),背部剃毛并用碘酚和75%酒精消毒,在脊柱两侧造4个直径10 mm的全层切口。将配方敷于创面,每2天保存30分钟,持续2周。12只雄性新西兰兔(1.8-2公斤)被用来验证疤痕的形成。将兔耳腹面软骨裸露麻醉,暴露耳腹面软骨形成4个直径为10 mm的伤口。然后将配方涂抹在创面上,前2周每2天维持30分钟。
细胞活力检测
将成纤维细胞接种于96孔板(每孔2000个细胞)中24小时,然后将培养基替换为无fbs培养基,并加入新鲜配方(相同当量浓度)24小时。然后使用细胞计数试剂盒-8 (CCK-8)孵育4小时,使用微孔板读取器在450 nm波长下测量光密度。细胞活力以百分数表示,与对照值归一化。
细胞吸收
将成纤维细胞接种于玻璃底培养皿中24 h,然后将培养基替换为含有不同配方的无fbs培养基,细胞孵育6 h。使用共聚焦激光扫描显微镜系统(CLSM, Leica TCS SP5,德国),使用VP荧光(425 nm激发,690 nm发射)和4 ',6-二氨基-2-苯基吲哚(4 ',6-二氨基-2-苯基吲哚(DAPI)荧光(405 nm激发,488nm发射)对细胞进行成像,以确定细胞摄取和定位。此外,收集经HA/VP-PLA处理的成纤维细胞,采用TEM标准方法,观察HA/VP-PLA的细胞摄取情况。
YAP抑制成纤维细胞的纤维化、增殖和迁移
将成纤维细胞接种于1 cm盖上8 h,然后用含有配方的培养基孵育24 h。细胞用多聚甲醛固定,并用Triton-100渗透。盖片依次与指定的一抗孵育过夜,并在室温下与异硫氰酸荧光素(FITC)偶联的二抗孵育2小时。最后,使用CLSM观察抗体定位和细胞结构。此外,通过western blot分析纤维化相关蛋白(TGF-β1和α-SMA)和增殖相关蛋白(PCNA)。对细胞迁移进行划痕试验。用垂直放置的移液管尖端垂直于水平线的背面形成划痕,并在含有配方的培养基中培养成纤维细胞48小时。
大鼠创伤再上皮化模型的评估
每4天采集一次伤口的数字图像,分析伤口的再上皮化情况。用过量戊巴比妥钠(150 mg/kg)对大鼠实施安乐死,16天后采集组织进行组织学评估。采用Masson和Sirius红染色进行组织病理学分析。使用ImageJ (version 1.48)软件定量天狼星红染色图像的红绿面积比。同时,分别对YAP、TGF-β、α-SMA和MMP-3进行免疫荧光分析。
兔模型瘢痕形成的评估
术后30天,用过量戊巴比妥钠对家兔实施安乐死,并制备组织进行组织学评价。组织切片横切疤痕最凸起部分,并用苏木精-伊红(HE)、Masson和Sirius红染色。采用疤痕高度指数(SEI,即疤痕高度与正常皮肤高度之比)评价疤痕形成情况。同时对TGF-β1、α-SMA、I型胶原、III型胶原分别进行抗体免疫组化染色。切片检查,使用扫描系统(ScanScope XT, Aperio, CA)扫描和计数免疫阳性细胞。
结果以平均值±标准差表示。统计分析采用学生t检验,使用Origin, p < 0.05为最低显著性水平。
摘要
介绍
方法与实验
结果与讨论
结论
数据可用性
参考文献
致谢
作者信息
道德声明
相关的内容
搜索
导航
#####
用电子显微镜对其形态特征进行初步研究。球形HA/VP-PLA嵌入可见HA网格中,根据TEM图像,HA链嵌入并包裹VP-PLA NPs(图1A)。低温透射电镜(cro - tem)图像显示,HA/VP-PLA由均匀的纳米颗粒组成,由于疏水VP和疏水PLA之间的相互作用,其结构有利于装载疏水VP(图1B)。此外,良好的分散性表明HA的两致病性可以提高HA/VP-PLA的稳定性。扫描电镜图像显示,HA/VP-PLA在HA凝胶基质中呈球形分布(图1C)。这使HA/VP-PLA具有足够的粘附力,可以直接应用于伤口,保持湿润的环境,并持续产生有效成分。
对HA/VP- pla的理化特性进行了广泛的研究,包括VP负载和降解。紫外可见光谱显示,VP被成功加载到HA/VP- pla上(图1D)。随后,通过测量VP和LA来研究HA/VP- pla的降解,包括VP释放和LA生成。大部分负载VP(28.3±2.2%)在12 h内释放。因此,HA/VP- pla中VP的EE与VP释放量相等,令人满意(图1E)。与先前报道的研究相比,HA/VP-PLA的释放速度更快(6 h vs. 40 h),这是因为PLA NPs中HA的结构可以促进NPs的分解释放VP,并发挥其水解降解特性[31]。正如预期的那样,LA含量随着时间的增加(6和12 h),验证PLA降解可以如预期的那样生成LA(图1F)。
综上所述,制备的HA/VP- pla具有独特的结构和物理化学特征,有利于VP、HA和LA的靶向递送,促进无疤痕伤口愈合。
图1
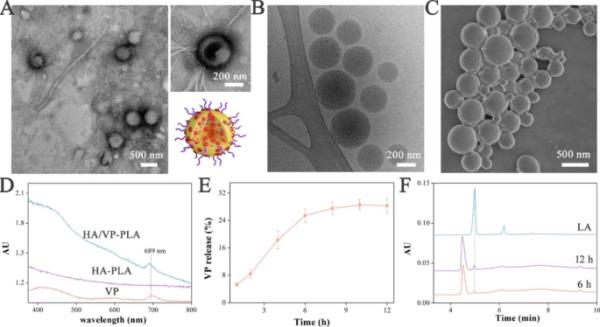
A: HA/VP-PLA的TEM图像及详细示意图;B-C: HA/VP-PLA的tem和SEM图像;D:紫外可见光谱(VP的吸收峰为689 nm);E:发布概要;F: LA检测的HPLC光谱(LA: LA标准,6和12:PLA降解6和12 h)
细胞生物相容性
HA/VP-PLA的生物相容性对其潜在的应用至关重要,并且HA/VP-PLA的更大的细胞摄取增加了YAP的抑制作用和细胞毒性。根据CCK-8测定,所有配方都表现出浓度依赖性的细胞毒性(图2A)。然而,在低VP浓度(< 2μg/mL)下,细胞毒性(细胞活力> 90%)不显著。在4μg/mL和6μg/mL时,HA/VP-PLA和HA- vp的细胞存活率分别为85-90%。然而,在8μg/mL时,细胞活力略有下降(< 85%的细胞活力)。相反,HA-PLA在任何浓度下均不影响细胞活力(细胞活力> 90%)。因此,HA/VP- pla具有良好的生物相容性,并使用2μg/mL VP进行下游细胞研究以平衡其细胞毒性和YAP抑制作用。
细胞摄取研究
用VP荧光法测定HA/VP- pla的细胞摄取。与VP-HA组相比,HA/VP-PLA组荧光更强,描绘细胞轮廓,荧光强度随孵育时间增加而增加(图2B)。此外,HA/VP-PLA在细胞膜和细胞质上形成了一些强烈的红色荧光点,表明丰富的HA/VP-PLA利用HA受体主动靶向细胞表面,并如预期的那样更有效地进入细胞。此外,透射电镜显示HA/VP-PLA显示均匀的黑暗,内体内部出现对比度增强(图2C)。这表明HA/VP-PLA很容易通过内体的封闭进入细胞[32]。然后,HA/VP- pla介导内核体降解,促进成纤维细胞内VP、HA和LA的释放。
YAP抑制,纤维化和增殖/迁移
研究YAP在处理后的成纤维细胞中的表达和核定位,初步确定HA/VP-PLA处理是否导致YAP抑制和纤维化抑制[33]。经处理的成纤维细胞免疫染色分析显示,HA/VP-PLA处理显著抑制YAP表达(图2D)。定量测定YAP荧光核胞质强度比表明,HA/VP-PLA在抑制细胞核积聚和改善YAP的胞质保留方面最有效(图2E)。这与细胞摄取研究相吻合。此外,PLA组分不影响YAP抑制作用。然后使用纤维化生物标志物研究纤维化抑制。Western blot结果显示,通过降低TGF-β1和α-SMA的表达,HA/VP-PLA抑制纤维化的效果最好(图2F)。随后,采用western blotting和细胞划痕法评估细胞的增殖和迁移能力,这两个在伤口愈合中起重要作用。在成纤维细胞的PCNA表达和迁移能力方面,HA/VP-PLA表现最好(图2F和G)。因此,HA/VP-PLA可以抑制YAP抑制纤维化活性,并传递HA和LA刺激增殖和迁移,有利于无疤痕创面愈合。
图2
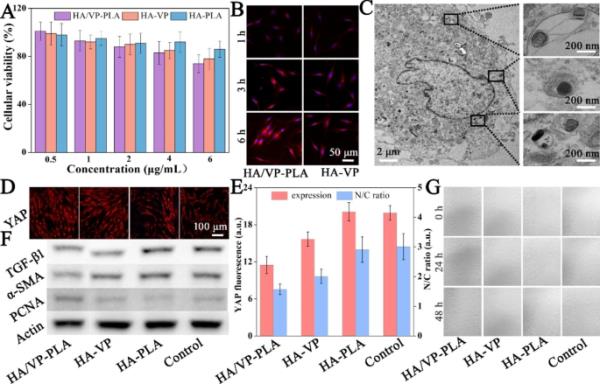
A:配方处理成纤维细胞的细胞活力;B: VP传递到成纤维细胞的CLSM图像;C: HA/VP-PLA处理成纤维细胞的超微结构观察;D: YAP表达的CLSM图像;E: YAP表达和核定位的统计分析;F:纤维化与增殖相关蛋白表达;G:划痕试验
HA/VP-PLA可促进大鼠创伤再上皮化。为了尽可能消除个体差异,我们将每只大鼠的4个创面分为制剂组和对照组,采用纳米凝胶涂抹创面,如图Fig. 3A所示。与对照组相比,配方显著改善了表皮再生,由于HA和LA的释放,HA/VP-PLA在伤口再上皮化方面表现最佳(图3B C)。
为了评估其抑制纤维化的潜力,我们分析了受伤后16天的伤口组织样本。在马松染色结果中,配方显著促进胶原沉积,加速伤口再上皮化。同时,Masson和Sirius红染色研究了新生胶原向成熟胶原转化、降低胶原I/III比值的胶原重塑。根据Masson染色,HA/VP-PLA促进胶原重塑,新生胶原(白色箭头区域)转化为成熟胶原(白色箭头区域),提高皮肤的机械强度[34]。然后,采用天狼星红染色法评价组织中的I型胶原(黄红色)和III型胶原(绿色)(图3E)。对照组胶原蛋白紊乱排列,以I型胶原为主。相比之下,HA/VP-PLA在改善胶原规则排列和增加胶原III含量方面表现最好,这是基于对胶原I/III比率的定量分析(图3F)。因此,HA/VP-PLA加速和改善创面再上皮化。
图3
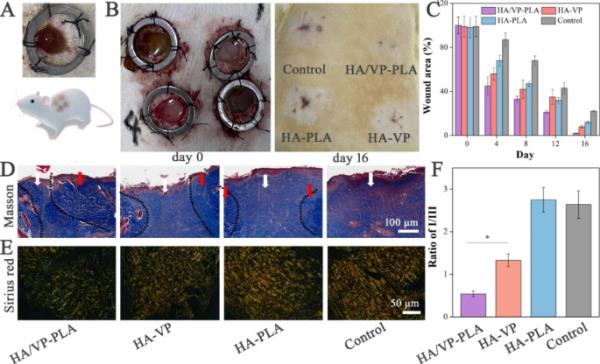
A: HA/VP-PLA在大鼠模型中的应用示意图;B:模型大鼠创面第0天和第16r天的再上皮化;C: 16 d各组创面面积百分比;D-E:组织Masson和Sirius红染色(白色箭头区域:新生胶原蛋白,红色箭头区域:成熟胶原蛋白);F: I型胶原与III型胶原比值的统计分析(*:p < 0.05)
体内免疫荧光分析进一步证实了YAP抑制和纤维化抑制作用。与其他配方相比,HA/VP-PLA在抑制YAP方面表现出最好的性能(图4A)。此外,TGF-β、α-SMA和MMP-3(影响胶原生成和代谢)的表达分别随着YAP的抑制而成比例地减少和增加(图4B - C)。因此,HA/VP-PLA通过其靶向递送能力抑制YAP,抑制纤维化,促进无疤痕伤口愈合。
图4
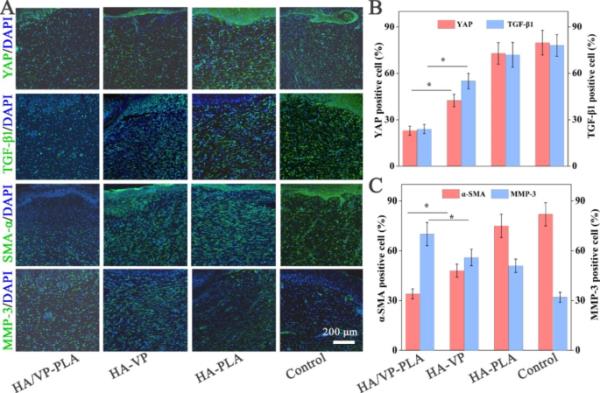
A:免疫荧光分析YAP表达和纤维化生物标志物;B: YAP与TGF-βα-SMA的统计学分析(*:p < 0.05);C: α-SMA、MMP-3的统计学分析(*:p < 0.05)
虽然大鼠模型提供了伤口再上皮化的信息,但由于缺乏机械张力,它们不能用于评估疤痕形成[35]。因此,我们将HA/VP-PLA应用于兔耳伤口模型,进一步评估其在控制瘢痕形成方面的潜力(图5A)。HA/VP-PLA在术后15天内促进兔模型创面上皮化,与大鼠模型相似。所有组织均较厚,术后30 d呈暗红色;HA/VP-PLA处理产生了最好的形态外观(图5B)。SEI用于评估疤痕厚度,并提供准确的证据,证明HA/VP-PLA可以显著控制疤痕的形成(图5C)。通过组织病理学分析评估瘢痕形成指标成纤维细胞增殖和胶原沉积(图5D)。苏木精和伊红(HE)染色分析成纤维细胞增殖显示,与其他组相比,HA/VP-PLA组成纤维细胞数量显著减少(图5E)。这一现象可以解释为HA/VP-PLA促进了细胞从增殖阶段向重塑阶段过渡[36]。
胶原沉积和HA/VP-PLA的Masson染色分析显示,胶原纤维沉积明显减少,胶原排列改善,结构纤细。进一步采用天狼星红染色评价组织中I型胶原和III型胶原,发现HA/VP-PLA改善了胶原排列,以III型胶原为主。I/III比率的统计分析表明,如预期的那样,HA/VP-PLA在降低比率方面更有效(图5F)。此外,HA/VP-PLA组细长的胶原在透射电镜下呈“篮织”状,排列规则,而对照组胶原排列杂乱,致密,粗大(图5G)。因此,胶原蛋白的超特征符合无疤痕伤口愈合[37]。
图5
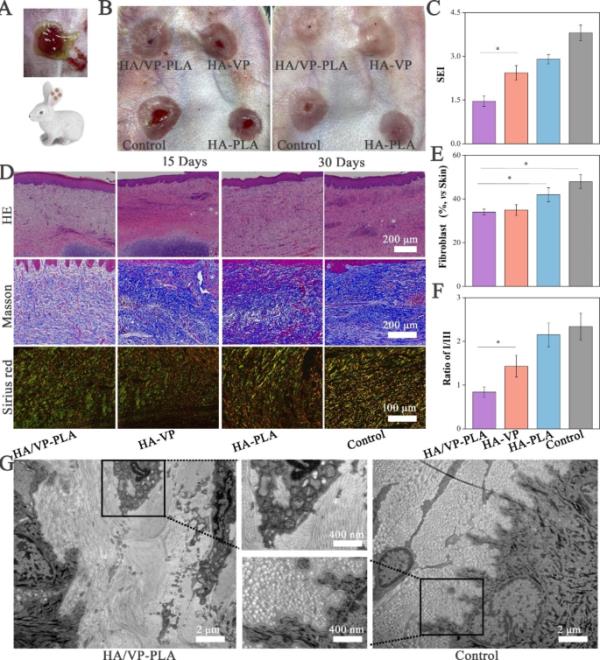
A: HA/VP-PLA在家兔模型中的应用示意图;B:术后15天和15天伤口组织外观变化;C:组织SEI统计(*:p < 0.05);D:组织HE、Masson、Sirius红染色;E:成纤维细胞增殖统计(*:p < 0.05);F: I型胶原与III型胶原比值的统计分析(*:p < 0.05);G: HA/VP-PLA组与对照组组织超微结构差异
通过免疫组织化学分析进一步研究纤维化相关蛋白的表达(图6A)。结果表明,HA/VP-PLA抑制TGF-β和α-SMA表达的效果最好(图6B)。HA/VP-PLA在减少I型胶原沉积和增加III型胶原沉积方面表现出更好的效果(图6C)。因此,兔模型研究证实了HA/VP-PLA通过抑制纤维化来控制瘢痕形成的巨大潜力。
图6
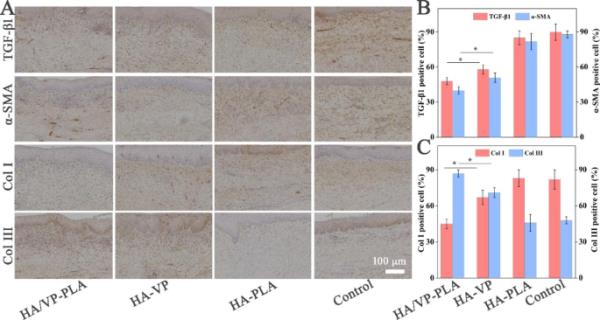
A:纤维化生物标志物免疫组化分析;B: TGF-β1与α-SMA的统计学分析(*:p < 0.05);C: I、III型胶原的统计学分析(*:p < 0.05)
综上所述,这些动物研究强烈提示,HA/VP-PLA可通过靶向递送,加速创面再上皮化,控制瘢痕形成,从而有效促进无疤痕创面愈合,抑制YAP,抑制纤维化,刺激成纤维细胞增殖和迁移。
开发了先进的HA/VP-PLA,以实现伤口组织成纤维细胞的靶向递送。它们通过加速伤口再上皮化和控制疤痕形成来促进无疤痕伤口愈合。发现HA和LA的持续释放可刺激成纤维细胞的增殖和迁移,加速伤口再上皮化。同时,HA/VP- pla成功地控制了疤痕的形成,因为抑制YAP的VP递送抑制了纤维化。使用成纤维细胞和动物模型的详细研究表明,HA/VP-PLA促进无疤痕伤口愈合的能力。因此,本研究为促进无疤痕伤口愈合提供了有效的治疗策略。未来的研究将为HA/VP-PLA的临床应用提供额外的实验基础。
下载原文档:https://link.springer.com/content/pdf/10.1186/s12951-023-02014-x.pdf
点击分享到