大多数植物在土壤中生长时与各种土壤微生物相互作用。豆科植物与根瘤菌的根瘤共生是土壤中植物与微生物相互作用的一种众所周知的现象。虽然显微观察有助于了解根瘤菌的侵染过程,但尚未建立监测根瘤菌与土壤生长根之间相互作用的非破坏性观察方法。在这项研究中,我们构建了缓生重氮根瘤菌菌株,它们组成性地表达不同的荧光蛋白,从而可以通过荧光团的类型来识别标记的根瘤菌。此外,我们还搭建了一个植物栽培装置——根际架(Rhizoframe),这是一个由透明亚克力板制成的填土容器,可以观察沿着亚克力板生长的根。结合荧光根瘤菌和Rhizoframe,我们建立了一个实时成像系统——Rhizoframe系统,使我们能够用荧光立体显微镜跟踪根瘤过程,同时保留根、根瘤菌和土壤的空间信息。利用Rhizoframe对不同荧光根瘤菌进行混合接种,实现了两株菌对单个根瘤混合侵染的可视化。此外,对表达生长素应答报告基因的转基因日本莲子的观察表明,Rhizoframe系统可以用于实时、无损的报告基因检测。因此,利用根框架系统有望加强对土壤中植物-微生物相互作用时空动态的研究。
大多数植物的生命开始于它们的种子与土壤接触的时候。根系是与土壤相互作用并吸收水分和养分的器官,在其生长过程中受到土壤物理、化学和生物环境的影响(Bengough et al. 2011;Karlova et al. 2021;Morris et al. 2017)。特别是,生物环境包括与各种土壤微生物的相互作用,包括共生细菌,如根瘤菌(Lambers et al. 2009)。我们在实验室中观察到的植物-微生物相互作用是在消除上述与土壤环境相互作用的条件下进行的(即,将土壤从根部冲洗并“清洗”以进行显微镜观察)。因此,我们还不能完全观察到在这一清洁过程中丢失的时空信息,如根部毛细胞附近的微生物与土壤接触的行为,微生物在根表面的定植,以及从定植到入侵宿主植物的转变。
豆科植物与根瘤菌的根瘤共生是植物与微生物相互作用的代表性现象。为了建立根瘤共生关系,土壤中的根瘤菌必须适应根瘤细胞。寄主植物感知到根瘤菌发出的信号后,会使根毛变形以诱捕根瘤菌,并形成管状结构,称为感染线,以便细菌侵入根内组织。根瘤菌在感染丝内分裂生长,同时诱导根皮质细胞去分化,开始分裂形成根瘤。感染线通过寄主的根毛向正在发育的根瘤原基延伸。最终,根瘤菌从感染线中释放出来,进入根瘤内细胞的细胞质。最后,定植在根瘤细胞中的根瘤菌将大气中的氮固定为氨(Kouchi et al. 2010;Oldroyd 2013;Roy et al. 2020)。
通过荧光蛋白的表达对标记根瘤菌进行显微镜观察,有助于我们了解这些感染过程(Fournier et al. 2008;计2002;Gage et al. 1996;Ledermann et al. 2015;Stuurman et al. 2000)。然而,以前的研究主要是使用从土壤中挖根的破坏性方法。在琼脂板上培养有时用于根瘤菌感染的延时成像。然而,这样的实验条件不能完全再现土壤中豆科植物与根瘤菌相互作用的动态。
植物改变其根系生长模式以有效地从土壤中吸收水分和养分(Lynch 1995)。在研究根系表型可塑性对环境变化的响应时,已经开发了无损测量技术来观察根系随时间的变化,而不破坏根系在土壤中的空间格局。例如,使用x射线计算机断层扫描和磁共振成像的3D成像方法可以可视化土壤中的根(Mooney et al. 2012;Rascher et al. 2011;Teramoto et al. 2020;van Dusschoten et al. 2016)。另一方面,为了观察靠近培养容器表面生长的根,广泛使用填土的透明箱或管进行植物栽培(Bengough et al. 2016;哈克和泰勒1982;judy et al. 2016;Neufeld et al. 1989;Zhao et al. 2022)。这些非破坏性方法主要侧重于测量根的大小和结构。作为最近的一个例子,GLO-Root系统利用表达基于发光的报告基因的植物,将土壤生长的根的结构和基因表达模式可视化(Rellán-álvarez et al. 2015)。他们还观察到拟南芥根系上假单胞菌的定殖。另一方面,在微观尺度上的观察对于了解微生物感染寄主植物根系的动态是必要的。另一个例子是,利用荧光报告水稻植株对土壤生长根系的丛枝菌根真菌感染进行了显微实时成像(Kobae and Fujiwara 2014)。该方法通过可视化植物分子标记间接显示丛枝菌根真菌的侵染动态。
本研究旨在建立一种利用荧光立体显微镜实时成像土壤中豆科植物与根瘤菌相互作用的无损观测系统。首先,我们构建了新的重氮效率慢生根瘤菌USDA 110菌株,该菌株组成性表达荧光蛋白,适合于根瘤菌的竞争感染分析。其次,通过优化根管的大小和厚度,构建了植物培养装置根际架(Rhizoframe),用于体视显微镜观察。通过结合这些工具,我们开发了根框架系统,使我们能够可视化土壤中根与根瘤菌的接触,并在立体显微镜水平上跟踪结瘤过程,同时保留了根、根瘤菌和土壤的空间信息。
PCR所用引物见表S1。对于荧光蛋白的组成表达,重氮菌USDA110的groEL4基因(blr5626)启动子区域(GenBank登录BA000040.2;基因组位置6,186,045-6,186,254)通过PCR从pBjGroEL4::DsRed构建中扩增(Hayashi et al. 2014)。根据慢生根瘤菌密码子频率对ZsGreen进行优化合成(图S1)。DsRed通过PCR从pBjGroEL4::DsRed构建体中扩增(Hayashi et al. 2014), tdTomato购自Takara Bio。每个荧光基因通过PCR扩增,引物在反向引物中含有trpA终止子(Wu and Platt 1978)。将GroEL4启动子和各荧光基因插入pK18mobsacB载体的EcoRI位点(Sch?fer et al. 1994),其中大霉素/链霉素耐药基因取代卡那霉素耐药基因。
对于染色体整合,B. diazoeffens USDA110的nifX下游区域(GenBank登录BA000040.2;基因组位置1,914,497-1,915,496)通过PCR扩增并插入pK18mobsacB载体的XbaI位点。用pRK2013作为辅助质粒,通过三亲本杂交将质粒转移到重氮效率WT B. USDA110上(figuski and Helinski 1979)。通过荧光和对多粘菌素和大霉素/链霉素的耐药性选择单交叉转偶联物。通过PCR和测序证实了nifX基因下游质粒的整合。
在HM盐培养基(Cole and Elkan 1973)中,添加0.1% (w/v) l -阿拉伯糖和0.025% (w/v) Bacto酵母提取物,28℃,140 rpm,相互摇动培养重氮菌。大豆(甘氨酸max (L.))稳定。简历。在300 ml的培养皿(CUL-JAR300, IWAKI)中,用无菌蛭石与Broughton and Dilworth (B&D)溶液(Broughton and Dilworth 1971)和B. diazoefficiens USDA 110 WT或荧光菌株在25°C的光照/暗循环下生长16 h。21 d后测定单株根瘤数、根瘤干重和乙炔还原活性(ARA)。
采用乙炔还原法估计固氮率(Hardy et al. 1968)。简单地说,将包括根瘤在内的根系从枝条上剪下来,放在100毫升的玻璃瓶中培养,玻璃瓶用橡胶塞密封,其中10% (v/v)的空气用纯乙炔代替。样品在25℃下孵育20分钟,使乙炔转化为乙烯。将1 ml顶空液注入装有火焰电离检测器的气相色谱仪(GC-2014 SHIMADZU, Kyoto, Japan)。乙烯通过与纯乙烯的标准曲线比较进行定量,并对进样量和孵育时间进行归一化。
用5% (v/v)次氯酸钠溶液对结节消毒3min,用无菌蒸馏水清洗10次。如前所述,从结节中提取总DNA (Shiro et al. 2016)。每个根瘤用100 μl无菌蒸馏水匀浆,然后用50 μl BL缓冲液(Shiro et al. 2016)加0.5 μl蛋白酶K (1 mg ml-1)处理24.5 μl匀浆。60℃孵育20 min, 95℃孵育5 min,离心后取上清作为PCR模板。PCR使用GoTaq G2热启动绿色主混合试剂(Promega),按照制造商的方案进行。PCR所用引物见表S1。
使用以下材料组装手工制作的Rhizoframe(图S2)。
透明亚克力板:宽100mm,厚1mm,高150mm,定制。亚克力板的底部不需要打圆。圆角时,用R=15.0 mm加工。
垫片:6毫米宽,3毫米厚,NICHIAS软密封(NICHIAS Co.)
防水双面胶带:5毫米宽,0.8毫米厚,高粘性双面胶带(3m日本有限公司)。
涤纶网孔:孔径38 μm,切成5 × 4 cm。
防水胶带:Ace Cloth 011单面密封防水胶带(Koyo Chemical)。
在YEM培养基中,28°C, 140 rpm的往复摇动培养loti中根瘤菌。根框架中填充了大约75毫升的土壤。将含有1 × 105根瘤菌的B&D溶液25 ml倒在土壤上。根框架用不锈钢盖覆盖,在25°C下静置3天。大豆(G. max cv。将Fukuyutaka或Enrei在25°C的无菌蛭石中黑暗萌发2天,然后转移到含有无菌蛭石的Rhizoframe或含有重氮白僵菌USDA 110的热处理颗粒土(无肥料土壤,Kanuma Sangyo Co.)中。根框架与不锈钢覆盖放置在一个水库,以湿润土壤。Rhizoframe植株在25°C光照16 h /黑暗8 h的条件下生长。将日本莲花(Regel) k.l larsen (Miyakojima mg - g)在24°C的琼脂板上黑暗萌发2天,第二天在16 h光照/8 h黑暗循环中萌发,然后转移到含有无菌蛭石的Rhizoframe中,其中含有M. loti MAFF303099。
使用轴向变焦显微镜Axio zoom V16 (ZEISS)进行显微镜观察。通过GFP过滤器(蔡司)检测GFP和ZsGreen,通过mRFP过滤器(蔡司)检测DsRed和tdTomato。使用ZEISS ZEN 3.3软件获取图像。
摘要
介绍
材料与方法
结果
讨论
数据可用性
参考文献
致谢
作者信息
道德声明
补充信息
搜索
导航
#####
为了可视化大豆与根瘤菌的相互作用,我们构建了大豆共生体B.重氮效率USDA 110菌株,该菌株组成性地表达三种荧光蛋白:ZsGreen, dred和tdTomato(图1a)。为了确保高荧光强度,每个荧光蛋白都位于BjgroEL4启动子的下游,该启动子在根瘤菌中组成性表达(Babst等,1996;Fischer et al. 1993;Hayashi et al. 2014)。据报道,重偶氮双歧杆菌在缺乏抗生素选择的情况下,质粒往往会迅速丢失(Stuurman et al. 2000)。因此,我们通过同源重组将荧光蛋白编码基因整合到重氮高效双歧杆菌USDA110的染色体中。我们将一个荧光蛋白基因整合到nifX的下游,nifX是负责固氮的nif基因保守簇的一部分(Hennecke 1990),预计与根瘤菌的感染能力无关。荧光根瘤菌根据荧光团的类型表现出不同的荧光强度。在红色荧光蛋白中,tdTomato菌株的荧光强度强于DsRed(图1a)。为了确定荧光蛋白整合对根瘤菌生长的影响,我们测量了每种荧光根瘤菌的倍增时间(图1b)。ZsGreen和DsRed菌株与野生型(WT) USDA110的倍增率相同。相比之下,tdTomato菌株的倍增时间比WT稍长。接下来,为了评估荧光蛋白整合对大豆根瘤共生的影响,研究了大豆和大豆之间根瘤表型的变化。检测“Enrei”和各荧光根瘤菌(图2a-d)。接种ZsGreen和DsRed菌株的植株形成成熟的根瘤(图2a)。它们的根瘤数、根瘤干重和ARA与接种了WT根瘤菌的植株相当(图2b-d)。tdTomato菌株在大豆上形成成熟的根瘤(图2a),而共生表型往往略低于WT(图2b-d)。为了比较荧光根瘤菌对WT的竞争能力,我们进行了混合感染试验。将荧光根瘤菌与WT约1:1的混合物接种到大豆中。同时,将混合的根瘤菌涂于琼脂培养基上,通过菌落计数法测定根瘤菌的比例(数据如图2e中的“接种量”所示)。21天后,计算每个菌株定殖的结节数(图2e)。各类型荧光根瘤菌在根瘤中的比例均不明显低于WT。同样,荧光根瘤菌之间的竞争也得到了检验。ZsGreen在根瘤中的百分比与DsRed相似,而tdTomato的根瘤占用率低于ZsGreen(图S3)。这些结果表明,细菌生长和共生特性都不受nifX下游荧光基因整合的影响。然而,BjgroEL4启动子对tdTomato的组成表达似乎对根瘤菌性能有轻微的负面影响。
图1
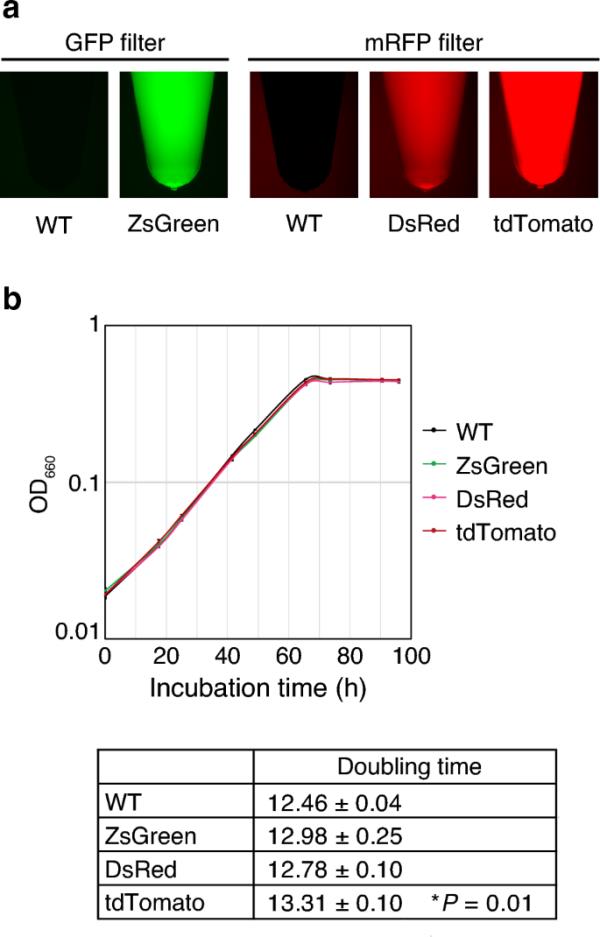
重氮梭菌USDA 110菌株组成性表达每种荧光蛋白的特征。a WT细胞悬液(OD660=0.5)和每个荧光根瘤菌(ZsGreen、DsRed和tdTomato)的荧光图像。分别通过GFP和mRFP滤镜获得相同曝光时间下的荧光图像。b WT与各荧光根瘤菌的生长曲线及倍增时间±SE (n=3-4)。通过记录培养基的光密度(660 nm)来测量生长情况。OD660值随孵育时间(小时:h)绘制。采用Dunnett 's检验确定与WT差异的显著性(*P < 0.05)
图2
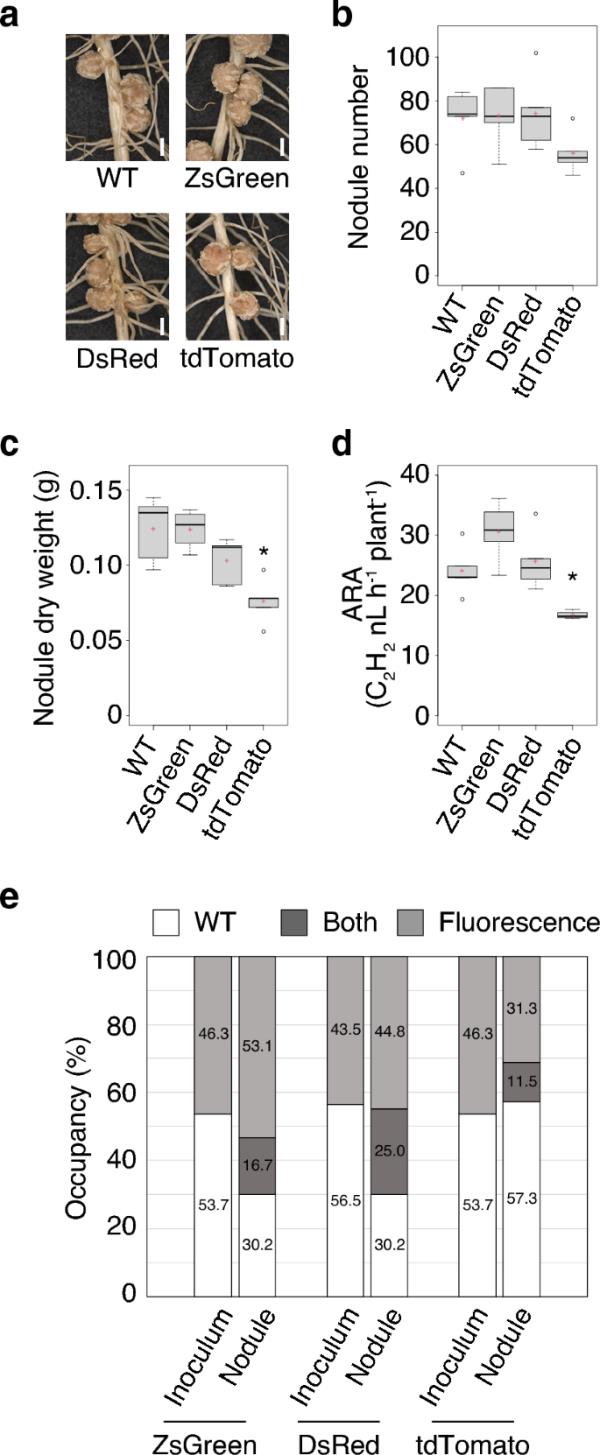
大豆cv接种后21 d的共生表型。Enrei接种了重氮高效B. USDA 110菌株,WT或突变菌株,每一个都组成性地表达荧光蛋白ZsGreen, dred或tdTomato。a结节形成,b结节数(n=5株),c结节干重(n=5株),d乙炔还原活性(ARA);N=4-5株)。比例尺=2mm (a)。在图b-d中,箱形图中的中心线表示中位数,上下四分位数界限用水平条表示。点表示异常值,红叉表示样本均值。采用Dunnett’s检验确定与WT的差异有显著性(*P < 0.05)。e WT与各荧光根瘤菌(ZsGreen、DsRed和tdTomato)共接种时的根瘤率;N=4株,96个根瘤)。用WT与荧光根瘤菌约1:1的混合物接种Enrei, 21天后,测定每个菌株的定植结节数。用PCR方法对结核中的每个菌株进行鉴定。“接种量”表示接种后根瘤菌在琼脂上形成菌落的比例(n=745-858个菌落)
我们修改了根管的大小和厚度,构建了适合体视显微镜观察的根框架(图3a)。根框是一个由1毫米厚的透明丙烯酸板制成的容器,底部有孔。容器宽100mm,厚7mm,高150mm,亚克力板之间留出5mm的空间,用于加土。在植物生长过程中,为了保护根系不受光照,在Rhizoframe外部安装了不锈钢盖(图3b)。将根框放置在一个蓄水池中,使其倾斜60°,这样根就可以沿着丙烯酸板生长(图3c, d)。蓄水池中加水以保持土壤水分。在丙烯酸板和Rhizoframe底部之间放置聚酯网(孔径38 μm)以覆盖孔,使植物吸收水分,同时将根保持在容器内(图3a)。在田间土壤中,当细长的植物根系与土壤接触时,感染事件就开始了。为了模拟田间土壤环境,我们将根瘤菌培养液倒在Rhizoframe的土壤上,并让其在土壤上沉淀3天。然后,将两天大的大豆幼苗转移到根瘤菌沉淀的根框架中(图S4a)。在培养过程中的任何给定时间,除去附着在Rhizoframe上的覆盖物,用显微镜观察根(图S4b)。通过丙烯酸板,可以对土壤中的根生长和根瘤形成进行无损观察(图3e)。根框栽培的大豆形成了许多成熟的根瘤(图3e、S5a),但根瘤数量低于盆栽栽培(图S5b)。
图3

根框,一种植物栽培装置,用于可视化豆科植物与根瘤菌的相互作用。a根框架的组成(从上到下:丙烯酸盒,聚酯网,丙烯酸板,螺丝)。b根框遮阳用不锈钢盖。c直立根架的蓄水池。d 14日龄大豆生长在根框内,倾斜60°。e根框接种后14天的根和根瘤。比例尺=3厘米。用市售材料组装的Rhizoframe如图S2所示
将培养装置(Rhizoframe)与荧光根瘤菌相结合,建立了根瘤菌体系。利用该系统,利用荧光立体显微镜捕捉了土壤中大豆根瘤共生动态的延时成像(图4a,电影S1)。接种5天后(dai),在根瘤菌定殖区观察到皮层细胞分裂(图4a;白色箭头)。皮层细胞的分裂导致结节原基的最初隆起,在那里观察到根瘤菌的入侵(图4a;6戴)。根瘤菌侵染区扩大,根瘤菌原基扩大,形成根瘤(图4a;8 dai, 10 dai)。在一个开放的箭头所指示的区域(图4a;5代),观察到表皮细胞上的根瘤菌定植和初始细胞分裂,而结节原基的形成停止(图4a;6、8、10)。我们还观察了土壤、根系和根瘤菌之间的相互作用(图4b, c)。在接种了荧光根瘤菌的Rhizoframe中,观察到根瘤菌分布在蛭石颗粒表面,特别是在层状结构的沟槽中(图S6a;箭头)。在播种植物的根框中,观察到根毛与根瘤菌沉淀的蛭石之间的接触(图4b)。此外,根瘤菌菌落在根表皮细胞上,包括根毛细胞上(图4c)。未接种土壤未观察到绿色荧光(图S6b)。
图4
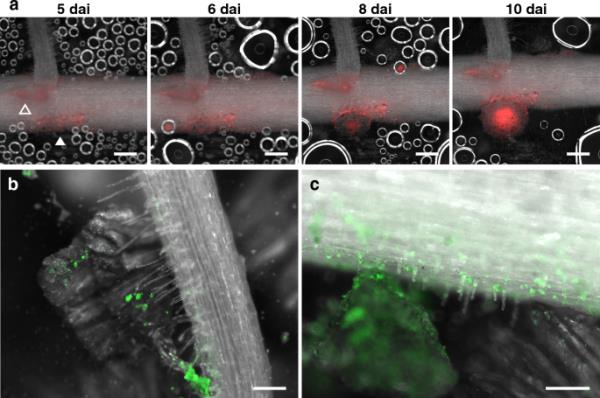
利用rhizframe系统可视化大豆与根瘤菌的相互作用。接种后5至10天的结瘤延时图像系列(dai)。箭头表示皮层细胞分裂发生的根区。b和c在7代用zsgreen标记根瘤菌接种A根和蛭石。荧光根瘤菌定位于蛭石颗粒、根表面和根毛细胞。大豆的简历。Fukuyutaka (a)或Enrei (b和c)接种重氮高效双歧杆菌USDA 110菌株DsRed (a)或ZsGreen (b和c),用荧光立体显微镜观察。红色和绿色荧光表明存在根瘤菌。比例尺=500 μm (a), 200 μm (b, c)
为了评估不同荧光根瘤菌菌株之间的侵染动态,我们用表达ZsGreen或tdTomato的USDA110菌株以1:1的比例接种大豆。小菌落形成于表皮和短根毛顶端6代(图5a;箭头)。很快,侵染线从短根毛中的微菌落中出现,侵染线在根毛细胞内分支并扩散(图5a;9 dai, 5b;箭头,S7a-c)。在我们的观察中,在根表皮上观察到的所有侵染线(n=80)都被单一荧光根瘤菌(7 dai)占据。我们还发现含有感染线的表皮细胞色素沉着(图5b, S7)。事实上,85%的表皮细胞,包括受感染的丝线(n=80),被观察到在根7周发生褐变。还观察到许多不能形成感染线的微菌落(图5a;箭头,5 b)。大多数根瘤仅被两种荧光根瘤菌中的一种定植,而有些根瘤被两种根瘤菌感染(图5c;箭头)。为了观察两个菌株同时感染单个结核的过程,我们对结核形成过程进行了延时成像(图5d)。在相邻的不同根毛细胞中观察到从ZsGreen菌株的微菌落延伸出的侵染线(白色箭头)和tdTomato菌株的侵染线(开放箭头)(图5d;7戴)。从10代开始观察到ZsGreen菌株侵入结节原基;ZsGreen菌株将其感染区扩展到结节中心直至14代。另一方面,tdTomato菌株在12代时在ZsGreen菌株的侵染区周围形成侵染区,并且在14代时侵染区扩展到ZsGreen菌株的侵染区周围(图5d)。
图5
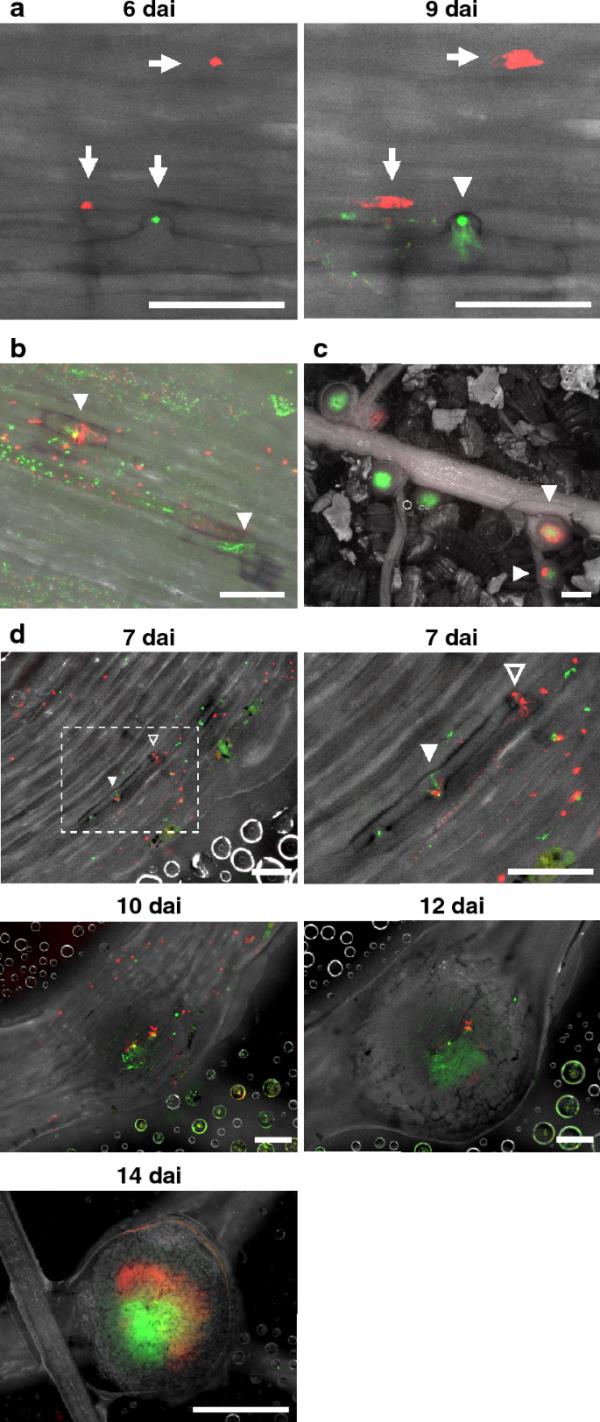
重氮白僵菌USDA110菌株ZsGreen和tdTomato混合接种后大豆结瘤的可视化研究。1个微菌落(接种后6天);代:箭头),菌落在表皮细胞上扩散(9代:箭头),根瘤菌通过感染线侵入根毛细胞(9代:箭头)。b感染线(白色箭头)在第9代有色素沉着的表皮细胞。两个菌株的多个菌落分散在根部。在感染线进入的表皮细胞中可见色素沉着。c根和结节在14节。在根瘤内定植的根瘤菌菌株可以通过荧光来区分。箭头表示由两种菌株定殖的结节。d 7 ~ 14天的结瘤延时图像序列。右上方的面板是虚线的放大视图。箭头表示感染线。大豆的简历。将Enrei与菌株ZsGreen和tdTomato(约1:1比例)共接种,在荧光显微镜下观察。绿色和红色荧光分别表示菌株ZsGreen和tdTomato的存在。比例尺=100 μm (a, b, d, 7 dai), 200 μm (d, 10, 12 dai), 1cm (c, d, 14 dai)
大豆是豆科植物的代表作物,但作为分子遗传分析靶点的技术发展仍然滞后。通过对两种模式豆科植物——L. japonicus和Medicago truncatula的研究,我们进一步了解了根系共生的分子遗传机制,包括根瘤共生(Harrison 2005;Kouchi et al. 2010;Xue et al. 2019)。因此,我们尝试利用Rhizoframe系统对枇杷结瘤进行延时成像。与在大豆中接种慢生根瘤菌类似,将表达DsRed (Maekawa et al. 2009)或GFP (Shimoda et al. 2020)的M. loti MAFF 303099在土壤中接种3天,然后将3天龄的幼苗转移到Rhizoframe中。由于枇杷植株比大豆小,每个根框内生长4株。到第3代,观察到卷曲的根毛和长长的侵染线穿过根毛生长(图6a),分枝的侵染线侵入根瘤原基(图6b)。随后,L. japonicus的根部形成了几个成熟的结节(图6c)。这些结果表明,根框架体系可用于日本松结瘤过程的无损分析。
图6
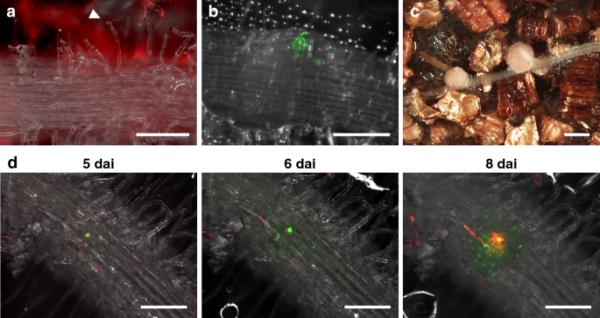
利用根框架系统可视化枇杷结瘤。a - c接种后3天(图a)、7天(图b)和14天(图c)的枇杷MG20植株结瘤情况。卷曲的根毛和感染线(箭头)。b分支感染线侵入结节原基。c根和成熟结节。d结瘤5 ~ 8天生长素反应模式的延时图像系列。在DR5::GFP- nls MG20转基因植株中,GFP信号(绿色)显示了生长素积累模式。红色(a、c、d)和绿色(b)的荧光分别表示存在组成性表达DsRed或GFP的罗氏分枝杆菌MAFF303099。比例尺=200 μm (a、b、d)和1mm (c)
接下来,我们研究了Rhizoframe系统是否也可以用于报告基因分析。作为报告者实验的一个测试案例,我们重点研究了根瘤菌感染期间生长素的反应。生长素是最著名的植物激素之一,在许多发育调控过程中调控细胞增殖和分化(Zhao 2010)。在根瘤共生中,研究表明皮质细胞中生长素的局部积累对根瘤原基的形成很重要(Suzaki et al. 2012)。在之前的研究中,在生长素响应元件DR5的控制下,建立了表达带有核定位信号(GFP- nls)的L. japonicus转基因植株(Suzaki et al. 2012)。在DR5::GFP- nls转基因植株中,生长素的积累可以通过GFP的表达间接监测。为了可视化生长素在结瘤过程中的反应,我们使用Rhizoframe将转基因DR5::GFP-NLS植株接种红色荧光M. loti,并实时成像生长素积累对根瘤菌感染的反应(图6d,电影S2)。在5代的根中,一些细胞表达了GFP,在GFP显示的细胞附近观察到短的感染线(图6d;5戴)。随后,感染线延长,细胞分裂进行,GFP表达增强(图6d;6戴)。在分化为结节原基的皮质细胞中观察到GFP的表达,根瘤菌以强烈的GFP信号侵入正在分化的皮质细胞(图6d;8戴)。这些观察结果显示生长素动态与根瘤菌感染实时同步,表明Rhizoframe系统可用于非破坏性报告分析。
标记的表达荧光蛋白的根瘤菌菌株是观察细菌动力学的一个有价值的工具。如果使用荧光蛋白作为监测植物中细菌活性的标记物,则荧光蛋白基因必须在被标记的细菌细胞增殖、集落形成和侵染宿主植物的整个过程中保持稳定。基于质粒的过表达已被应用于根瘤菌的荧光标记(Cheng and Walker 1998;Shimoda et al. 2020;Stuurman et al. 2000)。然而,据报道,在缺乏抗生素选择的情况下,质粒在某些根瘤菌物种中丢失,例如慢生根瘤菌(Stuurman et al. 2000)。目标基因的染色体整合能够克服质粒表达问题,并已成功应用于慢生根瘤菌(Ledermann et al. 2015)。转座子介导的随机转座和位点特异性同源重组用于将目标基因整合到染色体中。然而,由于转座子插入的位置不同,这种基因整合到染色体上可能会对细菌的生存能力产生不良影响。因此,本研究通过位点特异性同源重组将荧光蛋白基因插入根瘤菌的染色体中。作为整合的目标,我们选择了nifX的下游区域,这是一个在根瘤菌物种中保守的基因,最不可能参与根瘤菌的竞争力。事实上,nifX在自由生活状态下几乎不表达,只有在共生固氮活动时才高表达(Pessi et al. 2007)。我们的研究结果显示,ZsGreen和DsRed基因在该区域的整合不影响细菌生长(图1b)和共生特性(图2)。然而,tdTomato的组成性表达对根瘤菌性能有轻微的负面影响。由于tdTomato本身对细菌没有细胞毒性(Barbier and Damron 2016;Kong et al. 2016),根瘤菌性能的轻微下降可能是tdTomato过表达的影响,tdTomato是一种比其他荧光蛋白分子量更高的荧光蛋白串联二聚体(Shaner et al. 2005)。另一方面,大豆结节倾向于有轻微的绿色自身荧光。综上所述,基于我们对荧光标记菌株的评估,我们认为tdtomato标记菌株最适合于单次接种中观察感染动态,因为它在红色系列中显示出最亮的荧光强度。ZsGreen和dsred标记的菌株更好地用于评估它们竞争感染的能力,因为它们显示出相似的感染性(图S3)。
本研究建立了荧光根瘤菌与rhizframe相结合的显微镜观察系统,对土壤中根瘤共生进行无损实时成像。根管被认为是宏观水平上无损观察根系伸长动态的代表性装置(Bengough et al . 2016;哈克和泰勒1982;Neufeld et al. 1989;Zhao et al. 2022)。通过调整根管以适应体视显微镜观察台的尺寸,减小土壤厚度,构建了适合体视显微镜观察的根架。这些修改允许在微观水平上观察土壤-根-微生物的相互作用。虽然由于土壤变薄导致根际体积减少可能导致根瘤数量减少(图S5b),但每个根瘤发育正常(图S5a)。这些结果表明,Rhizoframe不会显著抑制根瘤共生,可以可视化根瘤菌对土壤和根毛的附着,感染线的形成,宿主细胞的根瘤菌定植和根瘤的发育,同时保留时空信息。
土壤包括岩石、矿物质、沉积物和有机物(Carson et al. 2009;Uroz et al. 2015)。这种马赛克组成为微生物提供了各种微栖息地(Hemkmeyer et al. 2018)。在本研究中,我们以蛭石为主要土壤载体,放置在根框中。众所周知,蛭石是根瘤菌的优良载体(Sparrow and Ham 1983),事实上,已有报道称蛭石表面形成根瘤菌生物膜(Fujishige et al. 2006)。Rhizoframe系统显示了荧光标记的根瘤菌在蛭石颗粒和与其接触的根毛上的定位(图4b, c)。土壤、根和荧光根瘤菌的同时可视化是我们系统的优点之一,可以用来了解土壤类型如何影响根瘤菌感染。
在感染之前,根瘤菌在根表面定植。其中一些根瘤菌形成微菌落,这是形成感染线的起点(图5a用箭头表示,5b)。特别是,在含有侵染线的表皮细胞附近容易形成大的微菌落(直径几μm)(图5b、S7a、d)。在侵染后,大豆根部短根毛细胞内形成了许多短侵染线(图5a、b、d、S7a - c)。它们的形态不同于在L. japonicus(图6a)中观察到的,也不同于在M. truncatula等其他豆科植物中报道的,在这些豆科植物中,长长的感染线通过根毛生长(Fournier et al. 2008;Liu et al. 2019;Rae et al. 2021)。据报道,根瘤菌通过困在短根毛和表皮细胞之间的微菌落的感染线感染大豆细胞(Rao and Keister 1978;Turgeon and Bauer 1985)。我们观察到的侵染线形成过程可能是大豆-慢生根瘤菌相互作用的主要侵染方式。虽然侵染早期在大豆根系上形成了许多侵染线,但大多数侵染线不能引导根瘤菌向寄主细胞迁移,也没有诱导出根瘤原基。只有少数感染线成功穿透根瘤原始细胞,形成根瘤(图5d、S7d)。据报道,侵染丝线的数量远高于在寄主植物上形成的根瘤数量(Gage 2004;Nishida et al. 2018),我们的观察也证实了这一点。在某些情况下,结节原基的形成在细胞初始分裂后停止(图4a;打开箭头,电影S1)。在根瘤共生中,结瘤自动调节(AON)是控制根瘤数量的主要负调控系统之一(Li et al. 2022;Oka-Kira and Kawaguchi 2006)。由于光合作用碳产物被用作共生固氮的能量来源,AON维持了获得氮源的收益和失去碳的成本之间的平衡(Nishida和Suzaki 2018)。AON受根瘤菌感染驱动,通过阻断感染线的穿透和皮层细胞的分裂来抑制根瘤菌的进一步结瘤。本研究中观察到的现象,如阻止感染线穿透和结节原基形成失败,可能是AON防止过度结瘤的一部分。未来利用Rhizoframe系统研究AON相关突变体和表达AON相关报告基因的转基因植物,将有助于了解这些观察结果是否与AON有关。
在对大豆根系的观察中,我们发现侵染丝线在微褐变的表皮细胞中频率较高。在明亮的视野中可以看到褐变,可以作为在荧光场下寻找含有感染线的细胞的标记。在许多情况下,由于褐变,表皮细胞的细胞壁部分可以清晰地观察到(图5a, b, S7)。与根瘤菌感染相关的细胞褐变早前有过报道(Vasse et al. 1993)。在这种情况下,含有感染线的表皮细胞附近的皮质细胞褐变与防御反应相关物质的积累有关,并抑制根瘤菌感染(Vasse et al. 1993)。相反,当我们从感染丝线形成阶段追踪结节时,所有结节(n=11)都来自褐变细胞中的感染丝线。这表明大豆根部表皮细胞的褐变可能是由不同的机制引起的,而不是由抑制根瘤菌感染所涉及的防御反应引起的(Vasse et al. 1993)。在根瘤菌与豆科植物共生的侵染过程中,根瘤菌释放的细胞壁降解酶促进寄主细胞壁的修饰,导致根瘤的形成(Gage 2004;Mateos et al. 2001;Roy et al. 2020)。在我们观察到的微菌落中,这种细胞壁修饰可能发生在与根表皮细胞接触的局部部位。在包含成功感染的被感染丝线的整个结节原基区域也观察到表皮细胞的褐变(图5d;12代,14代,7d)。综上所述,这些观察结果表明,表皮细胞的褐变可能是与结节发育过程中细胞壁重塑相关的一种反应。
利用Rhizoframe将ZsGreen和tdTomato菌株混合接种大豆,可以直观地观察到两个菌株对单个根瘤的侵染过程(图5d)。在这种情况下,每个根瘤菌通过不同的感染线进入宿主细胞。据报道,在紫花苜蓿和紫薇中,形成含有不同菌株的单一感染线(Gage 2002;Gage et al. 1996;Stuurman et al. 2000)。在我们的研究中,几乎所有在根表皮上观察到的微菌落和侵染线都是由单株荧光根瘤菌形成的(图5a, b, d, S7)。这些结果与之前对大豆的观察结果一致(Ledermann et al. 2015),可能是大豆根瘤菌感染的一个特征。在Rhizoframe系统中连续成像显示两种不同菌株在根瘤中的定殖速度存在差异(图5d)。在自然土壤中,存在着多种根瘤菌,它们总是为侵染寄主植物而竞争。阐明这种竞争侵染的机制将加深我们对根瘤菌共生能力进化的理解,有助于开发出能够克服本地根瘤菌侵染竞争和提供高接种效能的根瘤菌材料。除了通过接种单一根瘤菌来评估共生能力的传统方法外,最近的研究还侧重于通过根瘤菌合成群落的根瘤共生来分析根瘤菌菌株的竞争关系(Burghardt et al. 2018),以及通过混合接种基因盒或荧光标记根瘤菌(Bellabarba et al. 2021;Mendoza-Suarez et al. 2020)。这些方法有助于识别感染和占据单个结节的根瘤菌。另一方面,我们的Rhizoframe系统可以以一种无损和连续的方式捕捉根表面的感染竞争。在我们的系统中,几种不同的荧光标记根瘤菌的共接种具有揭示感染过程中感染竞争发生的优势。
利用Rhizoframe系统对表达生长素应答报告基因的转基因日本草进行观察,发现根系生长素动态与根瘤菌感染实时同步(图6d)。尽管一些研究报道生长素参与了结瘤(Hirsch et al. 1989;let et al. 2011;Rightmyer and Long 2011;Wasson et al. 2006),在结节发育过程中,生长素作用的时间和位置的特征很差。报告植物的创造促进了我们对生长素积累模式与根瘤发育之间关系的理解(Suzaki et al. 2012)。与之前的报道一致,通过根框系统观察到在感染线附近的少量细胞中有很强的生长素积累,并且皮层细胞活跃分裂(图6d,电影S2)。这些结果表明,根框架系统允许实时和无损的报告分析在土壤中,一个更自然的条件。先前的研究已经确定了调节根瘤共生的各种基因(Oldroyd 2013;Roy et al. 2020)。我们的系统有助于更深入地了解这些基因在结瘤过程中如何以及何时起作用。
利用Rhizoframe系统进行荧光立体显微镜的实时成像将使我们更好地了解土壤-根-微生物的相互作用,例如跟踪寄生微生物的感染过程和由此引起的根形态变化。然而,由于利用Rhizoframe系统可视化微生物需要荧光标记,因此如何观察难以转化的微生物的行为是一项重要的任务。我们期望进一步的想法来可视化以前隐藏的土壤,根和微生物的相互作用将扩大根框架系统的进一步可能性。
以下是电子补充材料的链接。
图书馆的src="http://58ziyuan.cn/news/93446/ / / e.video-cdn.net/v2/embed.js " > 补充档案2 (MP4 2712kb) 图书馆的src="http://58ziyuan.cn/news/93446/ / / e.video-cdn.net/v2/embed.js " > 补充文件3 (MP4 8557 KB) 下载原文档:https://link.springer.com/content/pdf/10.1007/s10265-023-01476-2.pdf










