饮食限制,如低血糖指数饮食(LGID),已成功用于治疗耐药癫痫。然而,这种饮食是否也可以抵消抗癫痫发生尚不清楚。在这里,我们研究了在潜伏的癫痫前期给药LGID是否可以阻止或延迟明显癫痫表型的出现。为此,我们使用了Synapsin II敲除小鼠(SynIIKO),这是一种颞叶癫痫模型,其癫痫发作在出生后2-3个月出现,提供了LGID可能影响癫痫发生的时间窗口。怀孕的SynIIKO小鼠在妊娠和哺乳期分别饲喂LGID和标准饮食。两种饮食在断奶小鼠中维持至5个月大。LGID仅在雌性SynIIKO小鼠中延迟癫痫发作并诱导癫痫发作严重程度降低。与癫痫表型平行,高密度多电极阵列记录显示,SynIIKO雌性海马中LGID的频率、幅度、持续时间、传播速度和间期事件的传播减少,而突变雄性则没有,证实了性别特异性效应。基于elisa的分析显示,LGID仅在女性中增加皮质-海马异孕醇酮(ALLO)水平,而对两性的ALLO血浆浓度均无影响。结果表明,LGID对癫痫发生过程的性别特异性干扰可归因于皮质ALLO的性别特异性增加,ALLO是一种已知可加强gaba能传递的神经类固醇。这项研究强调了开发一种基于性别的个性化颞叶癫痫治疗方法的可能性。
癫痫是最常见和最严重的慢性神经系统疾病之一,影响世界人口的1%,其特点是自发反复发作。癫痫发作是神经回路改变的附带现象,从最初的损伤开始,在一个被称为癫痫发生的潜伏过程中变得过度兴奋。最初的损伤会激活多个复杂的级联反应,持续时间从数小时到数月不等,包括神经退行性变、炎症活动、转录事件、神经发生、萌芽、神经元回路重组和神经胶质瘤[1,2]。通过神经可塑性的不适应机制,癫痫发生过程在第一次癫痫发作前逐渐改变神经元的兴奋性并改变电路的连通性[3]。尽管有大量能够抑制癫痫发作的抗癫痫药物(aed),但能够有效对照癫痫发生过程并预防癫痫的抗癫痫(AEG)策略仍然是有需求的[4]。
在过去的20年里,已经开展了几项基于使用常规aed预防癫痫的临床试验,但结果都不成功或存在争议,因此仍然缺乏有效的AEG药物来治疗高危人群[4,5]。这种失败的一个可能的解释是癫痫发生的分子机制不同于癫痫发作的表现。癫痫发作是明显兴奋性/抑制性失衡的产物,而癫痫发生则是导致失衡状况的复杂级联事件。AEDs的作用是试图恢复平衡,在大脑的其他地方产生相反的不平衡。相反,与癫痫发生相比,它可能是一种更有效的生理强化内在稳态过程,通常保护神经网络免受大脑损伤[6,7]。此外,对于表现出癫痫发生标志物且癫痫发作概率中等的易感患者,必须谨慎考虑使用aed对癫痫进行预防性治疗,例如在脑型疟疾的病例中,只有10%的儿童表现出明确的电体征会发展为癫痫[8]。因此,在癫痫发生概率不确定的人群中,必须考虑使用常规aed治疗产生副作用的风险,这使人们对这种用于预防/保护目的的治疗机会产生了严重的怀疑[4]。
以代谢为基础的疗法,如传统的高脂肪、低碳水化合物生酮饮食(KD)和耐受性更好的低血糖指数饮食(LGID)[9-11],可能是预防癫痫发展的另一种选择,因为它们在阻止耐药癫痫发作方面已被证明是成功的[12,13],而且相对没有副作用,因此可以对癫痫风险不确定的患者进行慢性治疗,即使是在儿科年龄。更重要的是,大量实验证据表明,以饮食为基础的治疗可以激活大脑中的多种稳态机制,从而提高癫痫发作阈值[14,15,16],并使神经元网络对压力源更具弹性[17],从而防止或逆转癫痫发作进展[18,19,20]。在这里,我们研究了LGDI在突触传递功能障碍引起的单基因反射颞叶癫痫的实验模型Synapsin II敲除小鼠(SynIIKO)中恢复癫痫发生过程的功效。
突触蛋白是由三个不同的基因(Syn1, Syn2和Syn3)编码的神经元特异性磷酸化蛋白家族,它们在大脑中大量表达,并集中在突触末端,通过调节神经递质释放而起作用[21-25]。对癫痫遗传易感位点的大规模研究发现,SYN2是导致人类癫痫易感性的五大基因之一[26]。这些发现得到了后续研究的支持,表明SYN2多态性与特发性全身性癫痫有关[27-29]。SynIKO和SynIIKO小鼠均表现出癫痫表型,包括部分继发性全身性强直阵挛性癫痫发作,在SynIIKO小鼠或双SynI/SynIIKO小鼠中更为严重[30-33]。重要的是,SynIIKO小鼠的行为癫痫发作具有晚发的特点,从而为测试LGID是否改变癫痫发生过程提供了一个操作窗口。
在本研究中,研究人员对SynIIKO小鼠在妊娠期和出生后5个月喂养LGID或标准饮食(StD)的行为和电生理进行了研究,以观察癫痫的出现和急性皮质-海马切片间期事件的存在。行为学和电生理结果显示LGID仅对SynIIKO雌性具有保护作用。基于elisa的分析显示,LGID喂养的雌性小鼠具有较高的皮质异孕酮(ALLO)水平,ALLO是一种神经类固醇,被称为gaba能传递的激动剂,这为LGID在颞叶癫痫小鼠模型中独特的性别特异性作用提供了机制基础。
SynIIKO小鼠通过同源重组产生,并在C57BL/6 J背景(Charles River, Calco, Italy)上广泛回交超过10代[30,34,35]。将每只纯合子SynIIKO雌性小鼠与一只纯合子SynIIKO雄性小鼠一起饲养在标准有机玻璃笼(33 × 13厘米)中,笼上铺有木屑,笼顶为金属。雌性SynIIKO小鼠被分成两组,从交配开始随意喂食StD或LGID[36])。两种饲粮(Bio Serv, Flemington, NJ)均为等热量(3.7 kcal/g),营养成分相同(碳水化合物65%,蛋白质20%,脂肪5%,纤维5%,水分5%),除了淀粉类型不同(淀粉是碳水化合物的主要来源)外,微量和大量营养素相同(补充表1)。LGID中的淀粉为70%直链淀粉和30%支链淀粉的组合(Hylon VII淀粉;而StD中的淀粉为100%支链淀粉(阿米卡淀粉;威彻斯特,伊利诺斯州)。
SynIIKO怀孕和哺乳期母鼠及其幼崽被随意喂食两种饲料(图1A)。断奶后,各组母鼠的雄性(M)和雌性(F)后代与母鼠保持相同的饮食(n=16 M StD, n=21 M LGID, n=14 F StD;n=12 F LGID)。样本量的选择基于以往SynIIKO小鼠行为癫痫发作的经验[31]。从断奶(P25)开始,每周检查每只小鼠的体重、食物摄入量、饮水量和癫痫发作情况。在5个月大时测定血糖和糖化血红蛋白(图1和补充图1 - 3)。小鼠在恒温(21±1°C)、相对湿度(60±10%)条件下维持12∶12 h的明暗循环(早上7点开灯)。所有实验均按照欧洲共同体理事会制定的指导方针(2014年3月4日指令2010/63/EU)进行,并得到意大利卫生部的批准(授权号600/2020-PR)。
图1
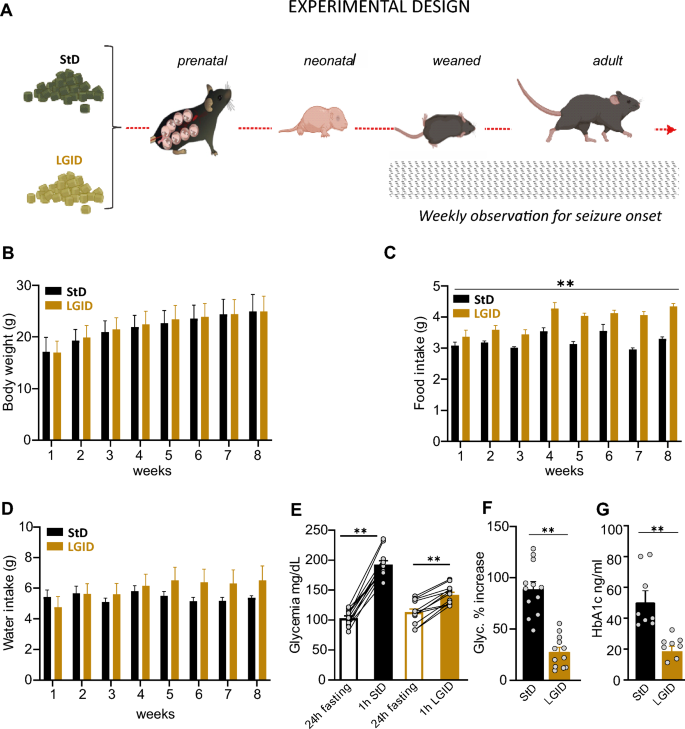
对两种饲粮饲喂期间的试验方案和参数进行了分析。从交配开始到怀孕和哺乳期间,对SynIIKO怀孕雌性随意提供StD和LGID。小鼠在断奶后和整个生命周期内也保持LGID。从断奶之日起,每周检查所有小鼠的体重(B),食物摄入量(C)和水消耗(D),持续两个月。对两个实验组的参数分析显示,LGID小鼠的食物消耗增加,但体重和水消耗没有差异(n=30 KO StD;n=32 KO LGID)。出生5个月后,对所有小鼠进行血液分析,评估血糖(E, F)和糖化血红蛋白(G)水平。E为了分析血糖,小鼠禁食24小时,在禁食后立即和给药后1小时测量血糖。在性病和LGID喂养的小鼠中,进食后血糖水平升高(性病和LGID均为n=12)。F进食后1小时血糖升高百分比(StD和LGID均为n=12)。与LGID处理的动物相比,StD喂养的小鼠的糖化血红蛋白水平更高(StD和LGID均为n=8)。数据以平均值±sem表示。*p < 0.05, **p < 0.01;双向重复测量方差分析(B-D),配对学生t检验(E),非配对学生t检验(F),非配对Mann-Whitney u检验(G)
每周的第一天(下午2点至4点),从断奶当天(P25)开始,在隔声动物饲养室进行癫痫发作挑衅。挑衅包括把动物从笼子搬到一个新笼子里。首先,打开盖子,抓住每只老鼠的尾巴,把它们举到旁边装有新鲜床上用品的笼子里。已知这一过程会引起SynIIKO小鼠的反射性癫痫发作[31,32,33,35,37]。所有挑衅行为都被安装在新笼子前的数码相机录了下来。随后,视频录像被传输到个人电脑进行数字存储,详细的癫痫行为分析是离线进行的。由于发作诱发和发作普遍性之间的时间间隔较短,我们没有使用严重程度评分量表,但根据先前描述的行为学描述[31,33]确定了癫痫发作的以下三个主要因素:(i)头部和身体肌阵挛性抽搐,包括退缩性口面部/前肢抽搐;(ii)全身性强直-阵挛性发作(伴或不伴跳跃),包括前位阵挛、前位阵挛、后位阵挛。跑步适应活动仅在少数动物中观察到,未包括在分析中。分析第一次观察到癫痫发作的潜伏期(从出生日期算起的天数)、每次癫痫发作的持续时间和跳跃动物的百分比。在行为随访结束时,处死5个月大的动物采集血液和大脑样本进行生化和电生理研究。
所有实验均在有症状(5月龄)的SynIIKO小鼠(雌雄不限)上进行。动物在斩首前用异氟烷麻醉,迅速解剖大脑,浸泡在冰冷的含氧“切割溶液”中,该溶液由(mM): 125 NaCl, 25 NaHCO3, 25葡萄糖,2.5 KCl, 1.25 NaH2PO4, 1 CaCl2, 2 MgCl2, 0.4抗坏血酸,2 NaPyruvate, 3 myo-肌醇组成,并以95% O2/5% CO2饱和。使用配备MicromCU65冷却装置(Thermo Fisher Scientific, Waltham, MA)的Microm HM 650 V切片机切割海马横向切片(300 μm厚)。切片在2°C高糖保护溶液中切割,高糖保护溶液含有(mM): 87 NaCl, 25 NaHCO3, 2.5 KCl, 0.5 CaCl2, 7 MgCl2, 25葡萄糖,75蔗糖,95% O2/5% CO2饱和。切片在35℃下孵育30-45分钟,室温下孵育至少1小时,记录标准溶液(人工脑脊液,ACSF)由(mM): 125 NaCl, 25 NaHCO3, 25葡萄糖,2.5 KCl, 1.25 NaH2PO4, 2 CaCl2, 1 MgCl2组成。在用于记录之前,切片在添加4-氨基吡啶(4-AP)的记录液中预孵育20分钟;200μM;西格玛奥尔德里奇,米兰,意大利)。然后将切片转移到“浸没”高密度多电极阵列(HD-MEA)记录室中,以1.5 ml/min的速率连续与ACSF添加200 μM的4-AP进行超滤。在整个实验过程中,监测浴槽温度并保持在33°C。
与体内自发性癫痫发作的罕见性一致,在控制灌注条件下,Syn IIKO小鼠的切片仅显示零星的自发性癫痫样活动。自发性发作的缺乏也与切片失传入和MEA记录的淹没模式有关。因此,SynIIKO片灌注K+通道阻滞剂4-AP,这是电压门控Kv1-Kv4钾通道亚型的广泛抑制剂[38-40],延长动作电位,从而增加突触前末端的神经递质释放[41]。在体外和离体制剂中,4-AP被广泛用于引起类似癫痫样的活性[42-45],正如先前报道的SynIIKO海马切片与野生型动物切片的关系[37]。
为了记录脑切片的电生理活动,我们使用Biocam X高密度cmos多电极阵列(HD-MEA;3Brain AG,瑞士)。该芯片集成了放大和模拟多路复用电路,以每通道18 kHz的采样率同时提供来自4096个电极(也称为像素)的细胞外记录。每个正方形像素的尺寸为21 × 21 μm,阵列集成了81 μm的电极间距(中心对中心)。像素按64 × 64阵列排列,产生5.12 × 5.12 mm的活动区域,像素密度为156.3像素/mm2。三个片上放大级提供60db的全局增益,带有0.1至5khz的带通滤波器。该带宽适用于记录慢速局部场电位(LFPs)和快速动作电位(APs)。收购使用Brain Wave软件(3Brain AG,瑞士)进行控制。每组记录10分钟的急性皮质海马切片,一旦活性稳定至少15分钟。4-AP (200 μM)的浴液应用[46]有利于诱导以自发峰波间隔放电(i - ic)为特征的癫痫样活动,这可以可视化为实时视频图像,其中视频帧的每个像素代表阵列的记录电极,并且根据颜色编码图具有与电压幅度相对应的颜色(参见补充图4B)。由单个记录像素记录的通常持续50 - 400毫秒的尖波复合体被命名为I-IC波,而由空间聚集的像素集合记录的时间聚集的I-IC波群被命名为I-IC事件。
脑波软件(3Brain AG)检测I-IC波,该软件采用先前描述的精确定时尖峰检测(PTSD)算法[47,48],该算法最初是为检测培养神经元产生的快速尖峰活动而定制的,并适用于检测较慢的局部场电位事件。为此,将阈值设置为噪声标准差的五倍,而不应期和峰值寿命分别设置为40和50 ms。为了评估LGID对I-IC波的影响,计算了振幅(波形模量的最大值)、持续时间(I-IC波熄灭所需的时间)和能量(I-IC波模量的时间积分)。
使用Pyton (v3.7.1)编写的自定义程序检测I-IC事件,该程序分析由BrainWave软件识别的I-IC波。对于I-IC事件的检测,我们初步评估了H(t)函数,该函数表示在所选组(G)的每个像素通道中检测到的I-IC波的时间聚集:
如下:
式中N(ta,tb)为(ta,tb)区间内I-IC波的个数,T为积分时间窗。H(t)在离散时间值t(0,?t, 2?t, 3?t…)计算,表示在以t为中心的时间窗口内检测到多少个I-IC波。对H(t)值应用阈值检测I-IC事件,并表示在皮质-海马切片的特定区域中与时间和空间相关的I-IC波的集合。I-IC事件可以定义为时间和空间相关的集合I-IC波,代表皮质海马切片特定区域内多个神经元聚集(即记录像素)的时间同步激活。在时间和空间上跟踪I-IC事件,以监测它们在片中的传播面积和速率。为了评估LGID对i - ic事件的影响,我们从记录中提取了以下特征:(i)受影响区域,即记录i - ic波的激活像素/通道数量与覆盖皮层或海马区域的像素/通道总数之间的比率;(ii)持续时间,作为检测到的事件的最后一个和第一个I-IC波之间的时间差;频率,即每分钟检测到的I-IC事件数;通过分析I-IC事件在空间和时间上的传播,得到了覆盖距离和传播速度。为了捕捉脑切片活动记录中发生的I-IC事件的传播特征,采用了计算机视觉方法。该算法由视频提取和多目标跟踪两个阶段组成。软件计算两个不同的值:一个是平均传播速度,即每条轨道的平均速度的加权平均值,其权重为每条轨道的持续时间;第二个是事件所经过的距离,计算为每条轨迹所经过的距离的总和。由于使用Pyton (v3.7.1)编写的基于自定义程序的算法,用于检测和分析I-IC事件和波的所有程序都是对实验者盲执行的。
在禁食24 h后,用迷你血糖仪(Accu-Chek Aviva, Roche)穿刺SynIIKO小鼠尾静脉,测量StD或LGID小鼠喂养1 h后的血糖浓度。血糖指数以血液样本的mg/dl表示。根据制造商的说明,使用HbA1c ELISA试剂盒(小鼠)(OKEH00661, Aviva System Biology, San Diego, CA)测量同一动物血清样品中的糖化血红蛋白(HbA1c)水平。所有标准品和样品一式两份。光密度值在450 nm处用多板读取器(Tecan Infinite?F500, Tecan Trading AG,瑞士)读取。HbA1c浓度以ng/ml表示。
分别饲喂StD或LGID的SynIIKO小鼠,在斩首后解剖皮质海马组织,立即称重并冷冻在液氮中,保存在- 80°C以待分析。根据阴道细胞学检查,所有雌性均处于发情期。采用有机相萃取法,乙腈溶解甾体,己烷去除脂肪和脂质。50 mg冷冻样品在冰上解冻,用聚四氟乙烯-玻璃均质机在15ml乙腈中均质。4℃,10000 × g离心10分钟后,将上清小心地转移到干净的玻璃管中,加入15 ml己烷,用力摇晃。通过分离漏斗收集有机相,重复两次除脂步骤。乙腈在旋转蒸发器(Rotavapor?R-100, BüCHI Labortechnik AG,瑞士)下蒸发至干燥,然后依次在浓缩离心机(VR-maxi St. a, Heto-Holten a /S,丹麦)中蒸发。干燥的样品在- 20°C冷冻,随后用于异孕酮(ALLO)的定量。使用DetectX ALLO免疫测定试剂盒(K044-H1, Arbor Assays, Ann Arbor, MI)根据制造商的协议测定ALLO浓度。将干燥的类固醇用一定量的乙醇和一定量的kit Assay Buffer按1:4 (v:v)比例溶解后,将样品大力摇动,并在室温下静置5分钟,以确保类固醇完全溶解。用试剂盒专用的Assay Buffer将样品体积中低于5%的乙醇带入后,立即对重组样品进行免疫分析。所有标准品和样品一式两份。在多板读取器(Tecan Infinite?F500)中读取450 nm处的光密度值。ALLO浓度值按组织重量和重构体积归一化,以pg/mg组织重量表示。
当n=样本量时,数据以平均值±sem表示。采用D’agostino - pearson正态性检验评估实验数据的正态分布。采用f检验比较两组样本间的方差。为了比较两个正态分布的样本组,使用未配对的学生t检验,如果两组的方差不同,则使用Welch校正。为了比较两个非正态分布的样本组,使用了Mann-Whitney的u检验。为了比较两个以上正态分布的样本组,我们使用了单因素方差分析,然后使用了Tukey事后多重比较检验。如果数据不是正态分布,则用Kruskal-Wallis检验代替单因素方差分析,然后进行Dunn事后多重比较检验。所有测试的Alpha水平均为0.5%(95%置信区间)。采用Prism软件(GraphPad software, Inc.)进行统计分析。
摘要。
介绍
材料与方法
结果
讨论
结论
数据可用性
参考文献。
致谢。
作者信息
道德声明
# # # # #
将雌性SynIIKO小鼠分为两组,任意饲喂StD和LGID。饮食从交配开始,哺乳期继续,断奶后在其整个生命周期(5个月)中喂养相同的饮食。从断奶之日(25d)开始的8周内,每周检查所有子代小鼠(雄性和雌性)的体重、食物摄入量和饮水量(图1A-D)。测量结果显示,lgid治疗小鼠的食物消耗量有适度但显著的增加,而体重或水消耗量没有增加。
通过使用LGID,我们期望维持低而稳定的血糖水平,并降低血糖峰值。因此,我们测量了所有SynIIKO小鼠出生后5个月的血糖和糖化血红蛋白(HbA1c)。为了研究这两种饮食对餐后血糖峰值的影响,在禁食24小时和禁食后1小时测量血糖(图1E, F)。在性病和LGID治疗的小鼠中,空腹血糖水平显示出相似的值。同时,与lgid喂养的小鼠相比,食物摄入诱导的葡萄糖水平升高明显更高(与禁食相比,增加百分比:~ 80%)(与禁食相比,增加百分比:~ 30%)(图1E, F)。我们还测量了糖化血红蛋白A1c (HbA1c)水平,该水平随时间推移整合了血糖水平[49],并一致发现lgid治疗的SynIIKO小鼠的HbAc1水平比以StD喂养的SynIIKO小鼠降低了两倍(图1G)。
从断奶当天开始,每周对行为癫痫发作进行测试,将小鼠置于隔离环境中并将其移动到新笼子中,这一过程已知可有效引发SynIIKO小鼠的反射性癫痫发作[30,31])。第一次癫痫发作的潜伏期在两个实验组之间没有差异(补充图1A),而LGID治疗的SynIIKO小鼠的总癫痫发作持续时间明显缩短(补充图1B)。所有小鼠都经历了由头、尾或腿的第一个短暂(5-15秒)快速肌肉抽搐(头部和身体肌阵挛抽搐,包括退缩的口面部/前肢抽搐)引发的全身性癫痫发作(补充图1C)。第二阶段是典型的强直-阵挛发作,持续时间在5到35秒之间(补充图1D),大约三分之一的小鼠出现跳跃,这是由特别强烈的阵挛肌肉收缩引起的(补充图1E)。所有癫痫发作均以持续时间从几秒到一分钟不等的癫痫发作后静止期结束(补充图1F)。当汇总男性和女性的数据时,行为癫痫发作的各个阶段不受饮食的影响(补充图1D-F)。然而,当雄性和雌性数据分开考虑时,LGID的显著影响仅在雌性小鼠中观察到,雌性小鼠的首次发作潜伏期较长,总发作持续时间缩短(图2A, B)。同样,雌性小鼠观察到强直-阵挛期持续时间和跳跃小鼠百分比的显著减少,而雄性小鼠则没有(图2D;E)。LGID的性别特异性疗效与食物或水消耗的性别差异无关(补充图2),也与LGID降低血糖或HbAc1水平的能力无关(补充图3)。
图2
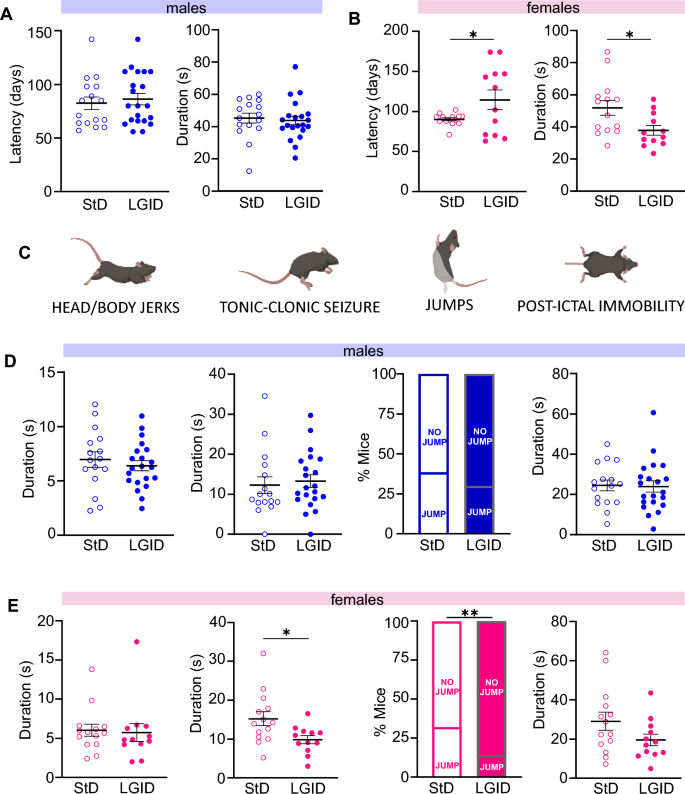
SynII KO雌雄小鼠首次观察到的癫痫发作分析。A, B雄性(A)和雌性(B)第一次发作的潜伏期和持续时间。雄性小鼠第一次发作的潜伏期和持续时间没有差异,而LGID治疗的雌性小鼠癫痫发作延迟和持续时间缩短。C分析了主要癫痫行为的代表性图像:头和身体抽搐、强直阵挛发作、跳跃和发作后不动。D、E癫痫发作的行为分析,包括(从左至右):头部和身体抽搐的持续时间,强直阵挛发作的持续时间,癫痫发作时跳跃的动物百分比和癫痫发作后不动的持续时间。这些参数显示,强直阵挛发作的持续时间和LGID治疗的雌性动物仅跳跃的百分比显着减少。数据表示为平均值±sem (n=16 M StD;n=21 M LGID;n=14F StD;n=12F LGID)。*p < 0.05, **p < 0.01;非配对学生t检验
皮质海马切片中的I-IC放电被认为是癫痫表型的代表[50],并且已经在SynIIKO小鼠中进行了描述[37]。我们在患有LGID或StD的5个月大SynIIKO小鼠的皮质海马切片中研究了这些癫痫的生物电标记。通过HD-MEA系统分析了I-IC活性,该系统允许同时从4096个电极进行高空间和时间分辨率的细胞外记录(补充图4A)。惊厥剂4-AP (200 μM;[42])应用于浴液中,有利于诱导以自发性峰波间期(I-IC)放电为特征的癫痫样活动。HD-MEA捕获的皮质和海马I-IC活动可以可视化为视频,其中视频帧的每个像素代表阵列的记录电极,像素的颜色对应于记录像素/电极检测到的电压幅度(补充图4B)。由每个记录像素/电极记录的尖波复合体(补充图4C)是一个“I-IC波”,而由空间聚集的像素集合记录的一组“I-IC波”代表一个“I-IC事件”(补充图4D)。
当所有SynIIKO小鼠进行比较时,无论性别,受I-IC事件侵袭的海马区域百分比不受饮食条件的影响。相反,该参数在lgdi处理的SynIIKO雌性小鼠中显著降低,而在相同饮食处理的雄性小鼠中没有受到影响(图3A, B)。当我们量化海马体I-IC事件期间激活的电极数量时,得到了类似的结果(图3C, D)。
图3
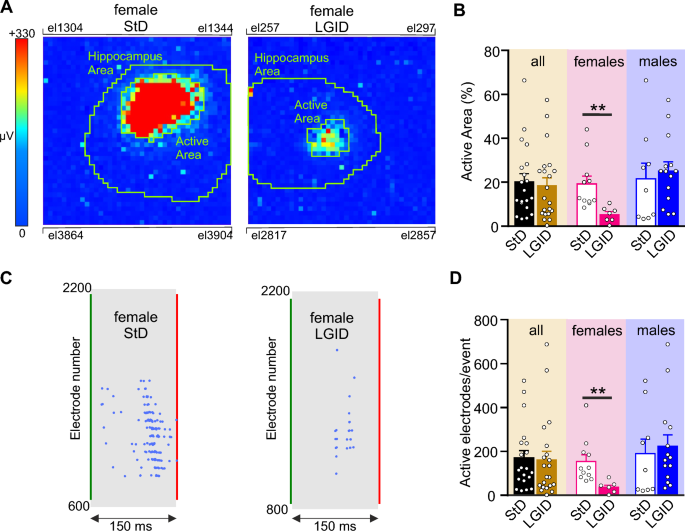
LGID对SynIIKO雌性小鼠海马I-IC事件的空间约束。两个视频帧显示了两只5个月大的SynIIKO雌性小鼠在性病(右图)或LGID(左图)治疗后的海马切片中激活的两个I-IC事件的彩色编码图。绿线划定了海马区。像素尺寸:81 μm宽。B条形图显示了所有(左)、雌性(中)和雄性(右)接受StD或LGID治疗的SynIIKO小鼠中,I-IC事件侵入海马面积百分比的平均值±sem和个体值。C .图a所示的两个I-IC事件的栅格图。在患有StD(左)或LGID(右)的雌性SynIIKO小鼠海马中记录的单个I-IC事件。每个蓝点代表由像素电极记录的I-IC波。绿线和红线分别表示I-IC事件的开始和结束。D条形图显示了所有(左)、雌性(中)和雄性(右)接受性病或LGID治疗的SynIIKO小鼠(性病和LGID治疗的SynIIKO小鼠n=20和21)在I-IC事件期间海马体切片中激活的电极数量的平均值±sem和个体值;StD和lgid处理的Syn II KO雌性小鼠n=11和7;n=9和14,分别用于StD和lgid处理的Syn II KO雄性小鼠)。**p < 0.01;非配对学生t检验
在所有接受lgid治疗的SynIIKO小鼠中,海马I-IC事件的频率显著降低,不分性别。然而,当在性别匹配的小鼠中比较该参数时,LGID诱导的I-IC率降低仅在雌性小鼠中仍然显着(图4A, B)。同样,当评估性别匹配或不匹配的SynIIKO小鼠海马I-IC事件的平均持续时间时,LGID仅在雌性小鼠中诱导I-IC持续时间显著降低(图4C, D)。
图4
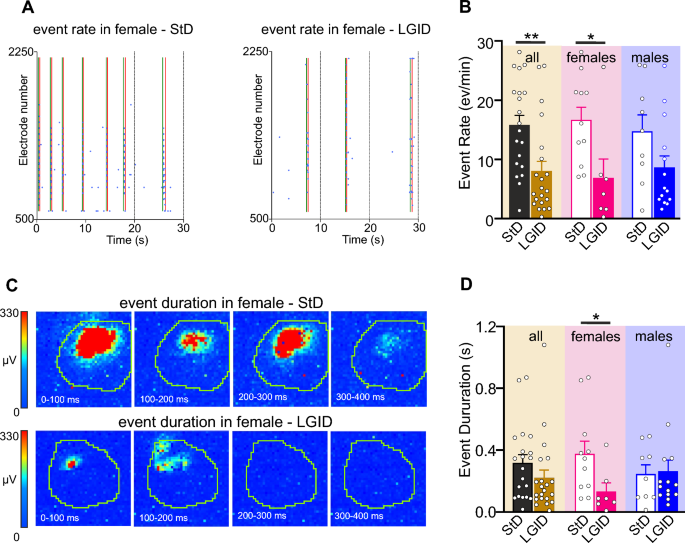
LGID减少SynIIKO雌性小鼠海马I-IC事件的频率和持续时间。具有代表性的栅格图显示了两个5月龄SynIIKO雌性小鼠在60 s的时间窗口内海马中检测到的各种I-IC事件,这些小鼠分别接受StD(左图)或LGID(右图)治疗。绿色和红色的线分别表示检测到的I-IC事件的开始和结束。每个蓝点代表由像素电极记录的I-IC波。B条形图显示了所有SynIIKO小鼠(左)、雌性(中)和雄性(右)在性病或LGID治疗下的海马切片中I-IC事件频率的平均值±sem和个体值。C两个系列的视频帧显示了两个5个月大的SynIIKO雌性小鼠的两个海马I-IC事件的彩色编码图,这些小鼠分别接受StD(上组)或LGID(下组)治疗。每个色码图被计算为100毫秒内振幅的变化,整个序列覆盖500毫秒的时间窗口。像素尺寸:81 μm宽。D柱状图显示了所有(左)、雌性(中)和雄性(右)感染StD或LGID的SynIIKO小鼠海马切片中I-IC事件持续时间的平均值±sem和个体值(在感染StD和LGID的SynIIKO小鼠中n=20和21);性病和lgid处理的雌性SynIIKO小鼠n=11和7;StD和lgid处理的雄性SynIIKO小鼠n=9和14;分别)。*p < 0.05, **p < 0.01;非配对学生t检验
我们还估计了每个I-IC事件的覆盖距离和传播速度,这些事件被理想化到一个单一的“质心”。同样在这种情况下,LGID治疗显著减少了I-IC事件的距离和速度,但仅在雌性SynIIKO组中(图5)。当我们测量尖波复合物(“I-IC波”)的持续时间和振幅时,得到了类似的结果;图6A),仅在LGID处理的雌性SynIIKO小鼠中,其持续时间和振幅再次显著降低(图6B, C)。
图5
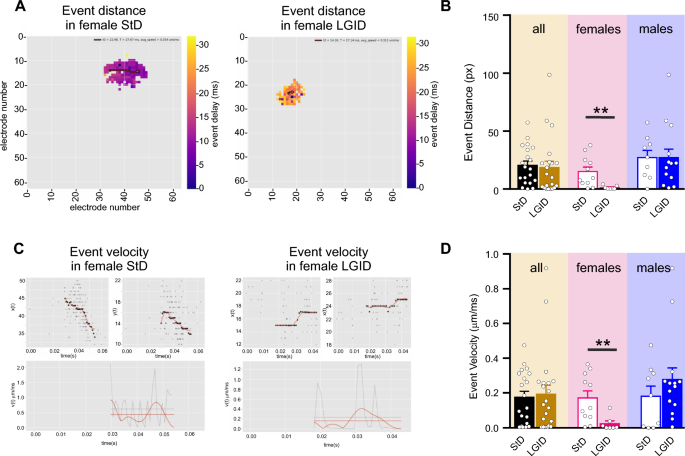
LGID降低了SynIIKO雌性小鼠海马I-IC事件的覆盖距离和传播速度。A两个视频帧代表两只5个月大的SynIIKO雌性小鼠,分别接受性病(左图)和LGID(右图)治疗。在延迟图上绘制的轨迹路径(红色)用于计算每个I-IC事件所覆盖的距离。填满的圆对应于轨迹的起点。B条形图显示了所有(左)、雌性(中)和雄性(右)患有StD或LGID的SynIIKO小鼠海马切片中I-IC事件覆盖距离的平均值±sem和个体值。C上面板显示了两个具有代表性的5个月大的SynIIKO雌性小鼠,分别接受StD(左图)和LGID(右图)治疗,每个I-IC事件在芯片的二维平面上的轨迹轨迹,分解为其水平和垂直分量。下图显示了I-IC事件的传播速度(红色水平线),这是通过对两只雌性小鼠分别接受StD(左图)或LGID(右图)治疗的每条轨迹的瞬时速度(灰色锯齿线)的平滑度(平滑红线)进行平均计算得出的。D柱状图显示了所有(左)、雌性(中)和雄性(右)感染StD或LGID的SynIIKO小鼠海马切片中I-IC事件传播速度的平均值±sem和个体值(在感染StD和LGID的SynIIKO小鼠中n=20和22);性病和lgid处理的雌性SynIIKO小鼠n=11和7;StD和lgid处理的雄性SynIIKO小鼠n=9和14;分别)。**p < 0.01;非配对学生t检验
图6
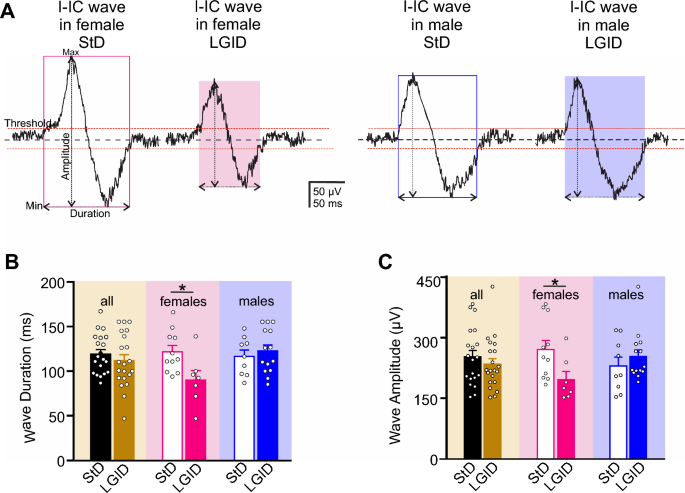
LGID减少SynIIKO雌性小鼠海马I-IC波的持续时间和振幅。在5个月大的SynIIKO雌性(左)和雄性(右)小鼠的海马体中记录有代表性的I-IC波电生理痕迹。B条形图显示了所有SynIIKO小鼠(左)、雌性(中)和雄性(右)在性病或LGID治疗下的海马切片中I-IC波持续时间的平均值±sem和个体值。C柱状图显示了所有(左)、雌性(中)和雄性(右)感染StD或LGID的SynIIKO小鼠海马切片中I-IC波振幅的平均值±sem和个体值(在感染StD和LGID的SynIIKO小鼠中n=20和21);性病和lgid处理的雌性SynIIKO小鼠n=11和7;StD和lgid处理的雄性SynIIKO小鼠n=9和14;分别)。*p < 0.05;非配对学生t检验
皮层癫痫样活动的HD-MEA记录突出表明,相对于在海马体中观察到的效果,LGID的疗效有所降低。LGID仅在减少事件率、事件持续时间和I-IC波持续时间方面有效,而与性别无关(补充图5)。然而,当在性别匹配的小鼠中比较这些参数时,事件和波持续时间的减少仅在雌性小鼠中保持显著,而在雄性小鼠组中则没有。
行为学和电生理数据均显示LGID对SynIIKO雌性具有性别特异性保护作用,提示饮食治疗可能调节与性别相关的神经类固醇通路。我们的研究重点是ALLO,众所周知,ALLO的抗癫痫作用归因于对GABAA受体的有效变构调节[51,52]。基于elisa的皮质海马组织提取物分析显示,ALLO浓度仅在lgid喂养的雌性中增加,而在lgid处理的雄性中不存在同样的效果(图7A)。这种影响仅存在于大脑中,因为LGDI不影响血浆ALLO水平,而与性别无关(图7B)。
图7
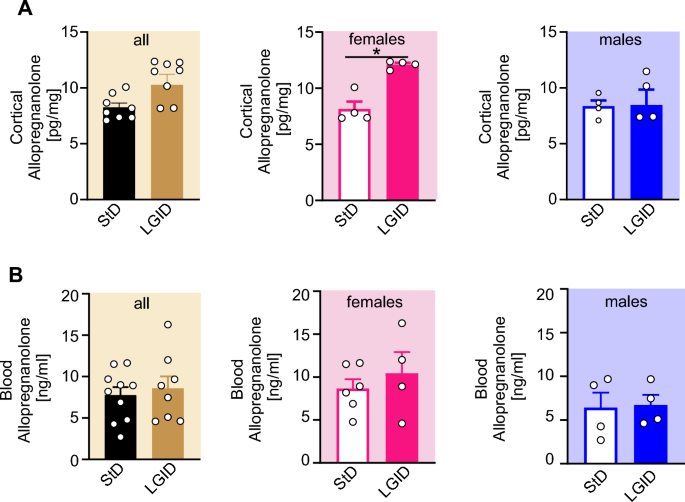
LGID增加雌性Syn II KO小鼠皮质ALLO浓度,而在雄性Syn II KO小鼠中没有。条形图显示了所有(左)、雌性(中)和雄性(右)分别饲喂StD和LGID的SynIIKO小鼠皮质海马组织(A)和血浆(B)中ALLO浓度的平均值±sem和个体值(分别为性病和LGID治疗的SynIIKO小鼠n=8和8);经StD和lgid处理的雌性SynIIKO小鼠n=4;在StD和lgid处理的雄性SynIIKO小鼠中n=4)。*p < 0.05;未配对曼-惠特尼u型检验
尽管进行了数十年的研究活动,但目前还没有一种fda批准的治疗方法能够真正预防高危人群癫痫的发展。使用aed获得的负面结果强烈地迫使人们转向新的干预策略[4,6,53 - 55]。由于患者群体的异质性,大多数AEDs旨在预防外伤性脑损伤或中风后癫痫的aeg试验也未能成功[56]。研究预防癫痫的新策略可能会利用癫痫遗传模型的表型同质性,其中癫痫发作要么是自发发生的,要么是对感觉刺激的反应。近几十年来建立的众多癫痫遗传动物模型[57]具有比任何其他癫痫实验模型更接近模拟绝大多数“特发性”癫痫综合征的优势[58]。因此,为了研究LGID的AEG作用,我们选择了SynIIKO小鼠,这是一种人类单基因癫痫性突触病,其致痫过程被我们和其他人广泛描述[25]。在该小鼠中,SynII的缺失诱导了GABA同步释放的上调,并伴随症状前小鼠中已经存在的延迟异步释放的丧失。由于GABA能突触外受体的激活,缺乏异步GABA释放会损害张力抑制,进而导致单个神经元和网络水平上的放电活动增强[37,59]。
饮食疗法治疗癫痫的历史相当悠久,希波克拉底已经记录了使用热量限制治疗癫痫[60]。生酮饮食(ketogenic diet, KD)作为一种治疗耐药癫痫的方法已有90多年的历史[13]。尽管疗效显著[61,62],但由于实施困难和耐受性,KD的使用仍然有限。最近,神经科学家提出了几种涉及代谢调节的抗癫痫治疗方法[15,63,64]。一种有效的替代饮食方法是LGID,在许多情况下其疗效与经典KD相当,但其耐受性要好得多[9,10,11,12,65,66]。因此,LGID可能更好地响应长期预防治疗的需求,以对照癫痫发生的健康患者,通常是儿童,有很高的癫痫发生概率。
在这里,我们测试了从产前开始在SynIIKO小鼠中早期应用LGID的体内和体外效果。行为特征显示,LGID在第一次癫痫发作的出现上产生了显著的延迟,并减少了其持续时间。令人惊讶的是,这种效应只在女性身上观察到。体外电生理研究证实了性别依赖性敏感性,显示只有雌性SynIIKO小鼠在喂食LGID后才出现诱发癫痫样活动的减少。这种特殊的影响不能归因于食物/水摄入量、体重、血糖指数或糖化血红蛋白浓度的任何性别差异。
LGID抗癫痫作用的作用机制是什么?虽然饮食限制被广泛用于治疗耐药癫痫,但其作用机制仍在研究中[5,16]。各种研究都强调,通过不同的低糖饮食(如KD、LGID或改良的Atkins饮食)或糖水解途径抑制剂(如2-脱氧葡萄糖(2DG))获得的神经元葡萄糖利用的减少是抗癫痫作用的共同机制[14]。有证据表明,高血糖会降低癫痫发作阈值[5,67],并且在KD治疗的患者中输注葡萄糖会导致癫痫发作的恢复[68],这进一步加强了这一假设。此外,抗糖尿病药物二甲双胍现在被认为是一种新的潜在的AED甚至AEG药物[69]。
在过去的20年里,低糖饮食的抗癫痫作用至少有三种不同的机制被确定[70]。最初有报道称,葡萄糖可用性的降低主要通过ATP敏感钾(KATP)通道干扰神经元的膜传导,KATP通道作为代谢传感器,将神经元的兴奋性与ATP水平耦合在一起[63,71,72]。事实上,胞质ATP浓度的降低具有由KATP通道打开介导的超极化效应[73]。最近,研究表明,糖酵解抑制导致细胞内NADH浓度降低,从而激活转录抑制因子REST/NRSF[15]。REST/NRSF的这种代谢募集可以诱导BDNF及其受体TrkB的转录抑制[15],并激活其他稳态途径[74]。事实上,REST/NRSF的表达和向细胞核的易位减少了神经元放电[75],减少了兴奋性输入,增强了抑制传递到兴奋性神经元[76,77]。最近也有研究表明,REST/NRSF可促进星形胶质细胞的K+缓冲和谷氨酸再摄取,这对维持突触内稳态至关重要[78]。
最后,一些研究小组报道,2dg诱导的糖酵解抑制通过增强神经元中戊糖磷酸通路(PPP)来促进NADPH的合成[79-82]。PPP是神经元中NADPH的主要来源[83],不仅通过2DG增强,而且在脑葡萄糖可用性降低[79]、禁食[84,85]或KD[86]的情况下也会增强。在这些情况下,葡萄糖被重定向到PPP, PPP代谢物的增加表明,可能是由于对NADPH的需求增加,旨在加强抗氧化防御。NADPH是5α-还原酶(5α-R)的关键辅助因子,而5α-R是ALLO生物合成的限速酶[52,87]。5α-R的n端与类固醇底物结合,而含有富含甘氨酸区域的c端与NADPH结合[88];因此,较高的NADPH浓度会增加神经元ALLO的产生[89]。ALLO也被称为内源性苯二氮卓类药物,作为突触和突触外GABAA受体的有效变构调节剂,因此增强了相位和张力抑制[90-92]。特别是,由带α/δ亚基的突触外GABAA受体介导的强直抑制对神经类固醇特别敏感,由此产生的强直传导增强有利于一种严格控制神经元网络兴奋性和癫痫易感性的分路抑制[93]。
鉴于在SynIIKO小鼠中发现的缺乏GABAergic强直抑制的促癫痫作用[37,59],我们关注脑ALLO水平的增加作为LGID抗癫痫作用的潜在机制及其性别特异性。我们观察到,与先前报道的na?ve啮齿动物大脑中的ALLO浓度一样,饲喂StD的雄性和雌性SynIIKO小鼠大脑中的ALLO浓度相似[94-96]。值得注意的是,LGID治疗只增加了女性皮质海马区的ALLO水平,而LGID对男女血浆中ALLO浓度没有影响。这些结果表明,LGID的性别特异性可能与外周ALLO水平的变化无关,而可能源于喂食LGID的SynIIKO雌性大脑中局部ALLO合成的性别特异性增加。
我们关于皮质ALLO的数据,虽然仍然是初步的,但为未来的研究指明了一条道路。为了找到lgid诱导的雌性皮质ALLO生成增加的机制解释,考虑以下因素至关重要:(1)雌性啮齿动物的血浆和皮质孕酮(PROG)浓度高于雄性,无论其发情周期如何[95,97];(2)大脑中由PROG通过5α-R的顺序作用合成ALLO,将PROG还原为5α-二氢孕酮(5α-DHP)和3α-羟基类固醇氧化还原酶(3α-HSOR),将5α-DHP转化为ALLO[98]。因此,PROG是酶级联反应的前体,由5α-R启动并限速,导致大脑中ALLO的生物合成[52]。
因此,未来的研究任务将是调查在雌性LGID喂养中,NADPH浓度的增加是否由于PROG的高可利用性而增强了5α-R活性和ALLO的生物合成,而在雄性中,由于PROG的有限可利用性,这种作用可能会大大降低或不存在。
性别特异性的其他原因,值得考虑的是5α-R活性和/或GABAA受体对ALLO的敏感性可能存在性别差异。事实上,先前的研究表明,雌性绿蜥的大脑比雄性表达更高水平的5α-R[99],雌性小鼠对ALLO的抗癫痫作用更敏感,因为雌性小鼠含有更丰富的突触外GABAA受体δ-亚基[100]。
预防癫痫是一项相关的科学挑战,也是一项尚未得到满足的迫切需求。在人类遗传性癫痫中,迄今为止还没有能够预防高危患者癫痫发展的治疗方法[3]。对由LGID治疗激活的体内平衡过程的功能机制的研究代表了确定新的治疗方案的一步。LGID延缓雌性小鼠癫痫发作的功效表明,这种高度可持续的饮食疗法不仅是一种抗癫痫治疗方法,而且可以预防或延缓具有不同病因的综合征的癫痫表型的出现,这些综合征具有相似的癫痫发生过程。最后,在女性中观察到的对LGID的更大保护,强调了开发个性化的针对性别的治疗的重要性。
以下是电子补充材料的链接。
ccDownload: /内容/ pdf / 10.1007 / s00018 - 023 - 04988 - 1. - pdf
点击分享到









